Конспект урока в 9 классе на тему «Соединения железа».
Цель урока: изучить свойства соединений железа (II) и (III), понять, какое практическое значение имеют эти вещества.
Задачи:
обучающие – сформулировать знания учащихся о свойствах гидроксидов железа (II) и (III), понимания различия этих свойств;
– добиться понимания взаимосвязи между соединениями железа со степенями окисления 2, 3;
– научить определять катионы ![]() и
и ![]() в растворе солей;
в растворе солей;
развивающие – развить умение сравнивать, обобщать, делать выводы;
– развить навыки самостоятельной работы с элементами исследования;
воспитательные – добиться осознания биологического и практического знания соединений железа.
Ход урока.
На прошлых уроках мы изучили строение и свойства железа – элемента побочной подгруппы.
На данном уроке наша цель заключается в изучении свойств соединений железа и осознании их биологического и практического значения.
– Вспомним, какие самые характерные степени окисления железа?
(ответы учащихся)
– Напишите два ряда соединений, образуемых железом со степенью окисления 2 и 3.
2 ученика работают у доски.
![]()
– Как вы думаете данные соединения одинаковы или отличаются по характеру и свойствам?
– Давайте экспериментально исследуем, чем отличаются соединения железа со степенью окисления 2, 3.
Для работы вам предлагается инструкция, которая поможет в исследовании.
Инструкция
Задание 1. Исследуйте свойства гидроксидов железа (II) и (III).
Опыт 1. Получение гидроксидов железа (II) и (III).
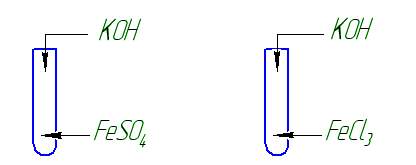
Что наблюдаете? Напишите уравнения реакций, выразите их сущность.
Опыт 2. Взаимодействие гидроксидов железа (II) и (III) с кислотой и щелочью. Взаимодействие гидроксида железа (II) с кислородом воздуха.
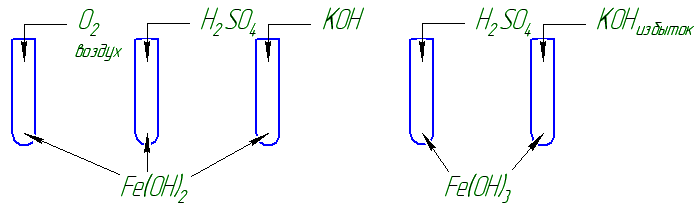
Что наблюдаете? Напишите уравнения реакций, выразите их сущность. Сформулируйте вывод о свойствах гидроксидов железа (II) и (III).
Задание 2. Исследуйте свойства солей железа (II) и (III).
Опыт 3. Качественные реакции на ![]() и
и ![]() .
.
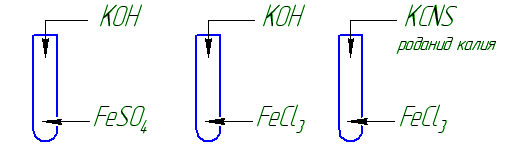
Что наблюдаете? Запишите уравнения реакций, выразите их сущность.
Сначала вы исследуйте свойства гидроксидов железа (II) и (III).
Давайте вспомним, как получить нерастворимые основания ![]() и
и ![]() .
.
(ответ ученика)
на доске заготовка
Гидроксиды железа
![]()
![]()
получение
![]()
![]()
свойства
![]()
![]()
![]()
![]()
Вывод: Вывод:
– Какую разницу Вы увидели в свойствах железа (II) и (III)?
– Сделайте вывод о свойствах этих соединений.
– С соединениями каких металлов Вы находите свойство в свойствах трехвалентного железа?
Итак, гидроксид железа (II), а соответственно и его оксид – проявляют, только основные свойства. Гидроксид железа (III), и его оксид – слабые амфотерные, с преобладанием основных.
А теперь посмотрите на поверхность ![]() и на стенки пробирки, в которой происходило взаимодействие
и на стенки пробирки, в которой происходило взаимодействие ![]() с кислородом воздуха . Что вы наблюдаете? С чем это связано?
с кислородом воздуха . Что вы наблюдаете? С чем это связано?
![]()
Как вы видите между соединениями железа со степенями окисления 2 и 3 существует взаимосвязь, – ![]() легко окисляется на воздухе – это говорит о неустойчивости соединения.
легко окисляется на воздухе – это говорит о неустойчивости соединения.
Если возможен переход от ![]() к
к ![]() , возникает вопрос: возможен ли обратный процесс?
, возникает вопрос: возможен ли обратный процесс?
– Что вы можете предложить?
![]() (ответы учащихся)
(ответы учащихся)
Железо образует два ряда солей. Некоторые соли существуют в виде кристаллогидратов.
на доске:
Соли железа
![]()
![]()
![]()
![]()
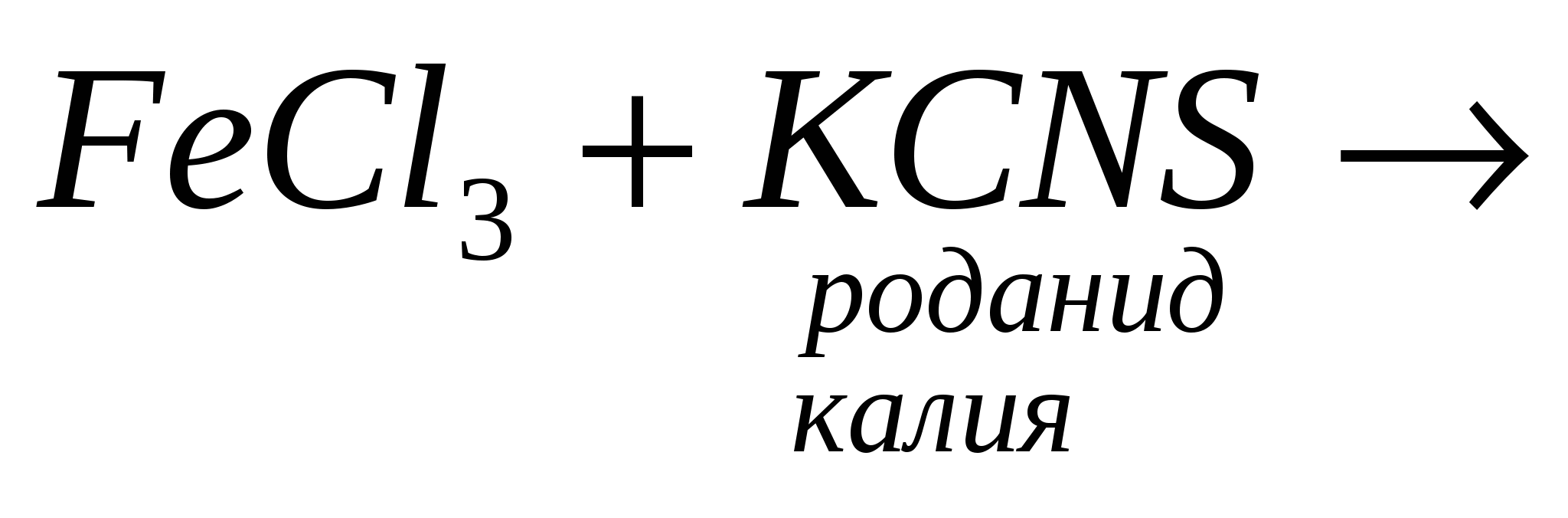
– Как можно отличить в растворе соединения железа со степенями окисления 2 и 3?
Для этого по инструкции выполните задание 2.
– Сделайте вывод.
Соединения II и III валентного железа имеют разное качественное определение. Соединения железа со степенью окисления 3 легко распознаются роданидами.
Соединения железа имеют важное биологическое и практическое значения.
Заслушаем сообщение об этом.
(доклад учащегося)
Ознакомившись с составом и свойствами соединений железа II и III выполните задания 1, 2 (кодоскоп).
Задание 1. На пиломатериалах из древесины иногда появляются пятна, обусловленные наличием в древесине солей хлорида и сульфата железа III. Какими опытами можно доказать, что эти пятна вызваны солями железа (III), а не гнилостными грибками и не солями железа (II)?
Задание 2. В состав некоторых сортов природного мела входит оксид железа (III). Предложите опыт для качественного определения содержания оксида в образце мела?
Оценки за урок…
Д/з: §53, Упр. 6-10 с 144.
