







Власова Надежда Ивановна
учитель физики
МКОУ Петропавловская СОШ
Тема урока
«Уравнение состояния идеального газа»
Тип урока: комбинированный.
Дидактическая цель: создать условия для восприятия, осмысления и первичного закрепления новой учебной информации об идеальном газе.
Задачи урока:
Образовательные: установление вида связи между макроскопическими параметрами состояния вещества и знакомство со следствиями, вытекающими из уравнения состояния идеального газа; формирование умений применять полученные знания при решении задач.
Воспитательные: создание условий для самостоятельного поиска решений проблемных ситуаций и проявления инициативы; формирование познавательного интереса к изучаемому материалу; формирование стремления к глубокому усвоению теоретических знаний через решение задач, воспитание чувства патриотизма и гордости за свою Родину.
Развивающие: развитие мышления и мировоззрения обучающихся через использование метода научного познания; осуществление межпредметных связей с математикой при выводе уравнения Менделеева — Клапейрона, развитие навыков самообразования.
Раздаточный материал: карточка для индивидуальной работы; домино для закрепления материала, папка «Учись учиться».
ТСО: компьютер, мультимедийный проектор, презентация к уроку, выполненная в программе Power Point.
Ход урока
I. Проверка знаний.
1.Организационный момент: приветствие, готовность к уроку.
2.Актуализация опорных знаний; мотивация учебной деятельности.
1.(Сообщение ученика)
Теплый воздух, водород и гелий применяют в летательных аппаратах: аэростатах, стратостатах, воздушных шарах и дирижаблях. Воздушные шары чаще используют в спортивных и научно-познавательных целях. Стратостаты предназначены для исследования верхних слоев атмосферы. Они находят применение в метеорологии, для запуска автоматических метеостанций. Управляемые аэростаты называют дирижаблями. Основные задачи, которые возлагаются на дирижабли сегодня,- перевозка грузов, укладка нефтегазовых труб, установка опорных линий электропередач, работа в труднодоступных районах, где нет дорог. В последнее время летательные аппараты используют еще и в рекламных целях.
2. (Дополнение учителя). (Слайд 1-7)
На слайде летательные аппараты.
Вы видите один из первых жестких дирижаблей «Цеппелин» -дирижабль 1890 года. Сейчас в летательных аппаратах используют в основном гелий, так как пожароопасность водородных летательных аппаратов резко ограничивает его применение как наполнителя.
Не всегда полеты названных аппаратов заканчивались благополучно. 30 января 1934 года в небо поднялся аэростат «Осоавиахим – 1». Он достиг рекордной высоты на тот момент – 22 км, но из-за плохой погоды обледенел и рухнул вниз. Погибли Андрей Васенко – конструктор, Илья Усыскин – физик и пилот Павел Федосеенко, наш земляк, уроженец г. Острогожска. Одна из улиц города носит его имя.
Тема сегодняшнего урока:
(Слайд 8).
«Уравнение состояния идеального газа».
(Слайд 9)
Цели:
Познакомиться с уравнением состояния идеального газа;
записать это уравнение в классическом виде;
сформулировать следствия, вытекающие из уравнения состояния идеального газа;
научиться использовать полученные уравнения при решении задач.
А чтобы достичь этих целей, повторим ранее изученный материал об идеальном газе.
1). Решить задачу по карточке (индивидуальная работа у доски).
Задача. Определить температуру, при которой тепловая скорость движения молекул водорода равна 2 км / с.
Дополнительный вопрос: «Какие микроскопические параметры характеризуют газ?»
Это масса молекулы, ее скорость, импульс и кинетическая энергия поступательного движения частицы.
Так как нам предстоит получить уравнение состояния идеального газа, давайте вспомним, что такое «идеальный газ». Это идеализированная модель, согласно которой считают, что: …
Перед вами слайд, на котором записаны 9 постулатов МКТ.
Все ли они верны для идеального газа? (Не верны 3, 6, 9)
Итак, верно ли, что …
(Слайд 10)
Модель «Идеальный газ»
В любом макроскопическом объеме газа число молекул очень велико.
Размеры молекул пренебрежительно малы по сравнению с расстояниями между ними.
Между молекулами существуют силы взаимодействия- силы притяжения и силы отталкивания.
Все соударения молекул являются абсолютно упругими.
Молекулы взаимодействуют друг с другом или со стенкой сосуда только в момент соударения.
Значительная средняя потенциальная энергия взаимодействия препятствует изменению среднего расстояния между ними.
Молекулы находятся в непрерывном хаотическом движении.
К движению отдельной молекулы применимы законы механики Ньютона.
Частицы колеблются около положений равновесия, взаимодействуя с ближайшими соседями.
2. Проверка знаний ранее изученных формул.
Учащимся демонстрируется слайд, на котором написаны формулы, но вместо некоторых величин стоит знак ?. Заменить знак ? недостающими буквами.
Слайд 11
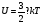
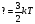
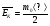
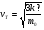
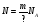
Учащиеся дописывают формулы.
Демонстрируется слайд с правильно записанными формулами.
(Слайд 12)
Формулы.
1.Зависимость внутренней энергии идеального газа от температуры.
2.Средняя кинетическая энергия поступательного движения одной частицы.
3.Средняя кинетическая энергия молекул с массой m.
4.Тепловая скорость движения молекулы.
5.Число частиц в газе.
.Ученики проверяют правильность написанного по слайду и называют, что можно определить по той или иной формуле.
Проверка решения задачи, выполненной индивидуально у доски.
Дано: Решение.
Н2 υТ=√3kT/m
υT=2.103 м/с υТ2=3kТ/m
M=2.10-3 кг/моль υТ2.m=3kT
T=mυT2/3k
m=M/NA
t — ? T=MυT2/3kNA
T=322 K
Ответ: t = 49 С
II Содержание нового материала.
Итак, газ характеризуют его микроскопические параметры. Это индивидуальные характеристики молекул: масса молекулы, ее скорость, импульс и кинетическая энергия поступательного движения; концентрация молекул.
Макроскопические параметры газа – величины, характеризующие газ, как физическое тело: температура, объем, давление газа.
Одна из важнейших задач МКТ – установление связи между макроскопическими и микроскопическими параметрами газа.
А мы сегодня получим связь между макроскопическими параметрами.
Слайд 13
Уравнение состояния вещества
Уравнение, выражающее связь между макроскопическими параметрами состояния вещества (р, V и Т), называется уравнением состояния этого вещества.
В общем случае эта задача является очень сложной и до сих пор не решена. И только для идеального газа получено решение этой задачи.
Слайд 14
Уравнение состояния идеального газа
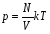
Получим это уравнение в классическом виде. Для этого параметры p, V и Т поместим в левую часть уравнения, а остальные величины – в правую. Один ученик преобразует уравнение у доски, остальные на месте.
1.Умножив обе части уравнения на V, получим: 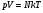
2.Обе части уравнения разделим на Т: 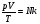 -это соотношение в 1834 г. было получено французским физиком Бенуа Клапейроном. Но оно неудобно к применению, так как в него входит неизмеряемое на опыте число молекул N.
-это соотношение в 1834 г. было получено французским физиком Бенуа Клапейроном. Но оно неудобно к применению, так как в него входит неизмеряемое на опыте число молекул N.
3. Вместо N в полученное выражение подставим: N =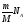 .
.
4.Уравнение теперь имеет вид: 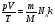 (Слайд 14)
(Слайд 14)
5.Найдем произведение NA и k:
NA. k = 6,02.1023 моль-1 . 1,38.10-23Дж/К= 8,31 Дж/ (моль. К)
Мы получили универсальную газовую постоянную R.
(Слайд 15)
Универсальная газовая постоянная R
NA.k = R
R = 8,31 Дж/(моль.К)
Итак, после преобразований уравнение имеет вид:
Слайд 16
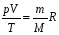 — уравнение Менделеева-Клапейрона
— уравнение Менделеева-Клапейрона
В таком виде уравнение состояния идеального газа представил Дмитрий Иванович Менделеев в 1874 году, обобщив результаты Б.П. Клапейрона.
Слайд 17
Дмитрий Иванович Менделеев – великий химик, физик, педагог. (1834 – 1907)
Этот портрет (на слайде) написал наш земляк И.Н. Крамской.
Интересно знать, что наполненный водородом шар одним из первых использовал для научных целей Д.И. Менделеев. В 1887 году он поднялся на воздушном шаре для наблюдения солнечного затмения.
Уравнение Менделеева-Клапейрона справедливо для идеального газа любого химического состава. Единственной величиной, определяющей специфику газа, является молярная масса. Из уравнения состояния идеального газа вытекает ряд важных следствий:
Слайд 18
Закон Авогадро. 1811 г.
При одинаковых температурах и давлениях в равных объемах любых идеальных газов содержится одинаковое число молекул.
Доказательство.
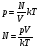
Закон Авогадро впервые был сформулирован в 1811 году итальянским ученым Амедео Авогадро. Долгое время это утверждение не было законом, А всего лишь гипотезой, в которую мало кто верил. И только по истечении 50 лет его гипотеза стала законом благодаря ученому Клаузиусу, который вернул имя забытого Авогадро в науку.
Слайд 19
Закон Дальтона 1801 г.
. Давление смеси химически не взаимодействующих идеальных газов равно
сумме парциальных давлений этих газов.
p = p1+…+pn
Парциальным называют давление, которое имел бы газ, входящий в состав газовой смеси, если бы он один занимал объем, равный объему смеси при той же температуре.
Английский школьный учитель Джон Дальтон, ставший замечательным физиком и химиком, членом Лондонского королевского общества, образование получил самостоятельно. А в 1801 году открыл закон парциальных давлений, носящий его имя.
.
Слайд 20
Объединенный газовый закон. 1824 г.
Отношение произведения давления и объема идеального газа к его абсолютной температуре, есть величина постоянная для данной массы газа.
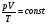
Этот закон был впервые получен в 1824 году Сади Карно – французским ученым. И этот ученый вначале не был замечен. И только Клапейрон обратил внимание на выводы Карно и представил этот закон в виде:
Слайд 21.
Уравнение Клапейрона 1834 г.
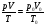
p0, V0 , T – параметры начального состояния газа,
p, V, T — параметры конечного состояния газа.
Итак, мы получили уравнение состояния идеального газа в классическом виде – уравнение Менделеева – Клапейрона и следствия для данной массы данного газа.
Для чего нужно уравнение состояния? Не только идеальный газ, но и любая реальная система – газ, жидкость или твердое тело – характеризуется своим уравнением состояния. Но только эти уравнения намного сложнее, чем уравнение Менделеева-Клапейрона для идеального газа. Знать уравнение состояния необходимо при исследовании тепловых явлений. Уравнение состояния позволяет определить одну из величин, характеризующих состояние, например температуру, если известны две другие величины. Это и используют в термометрах.
Зная уравнение состояния, можно сказать, как протекают в системе различные процессы при определенных внешних условиях, например, как будет меняться давление газа, если увеличивать его объем при неизменной температуре, и т.д. Речь уже идет о газовых законах, которые активно работают в живой природе, широко применяются в медицине, газообмен в легких у животных и у человека происходят тоже в соответствии с газовыми законами.
Но об этом поговорим на следующих уроках.
Закрепление
А теперь проверим, как усвоили вы новый материал.
Слайд 22
Дорога к знанию? Ну что ж, ее легко понять.
Ответить можно сразу:
Вы ошибаетесь, и ошибаетесь, и ошибаетесь опять,
Но меньше, меньше, меньше с каждым разом!
2. Проверим усвоение изученной темы с использованием дидактической игры «Домино».
Ученикам предлагается комплект физического «домино» по теме урока. Они отыскивают карточку №1 (в данном случае с вопросом «Что называют молярной массой?» и ищут на ее вопрос в общей массе карточек домино карточку с ответом; найдя, приставляют ее к первой карточке. На правой стороне приложенной карточки написан следующий вопрос, к которому учащимся опять нужно найти карточку с ответом, и т. д. Получается следующая «цепочка»:
|
Что называют молярной массой? | |
|
Молярной массой называют массу одного моля вещества |
Чему равно нормальное атмосферное давление? |
|
Нормальное атмосферное давление равно 105 Па |
Перечислить макроскопические параметры состояния идеального газа |
|
Макроскопические параметры: р – давление, V – объем, Т — температура |
Перечислите единицы измерения давления, объема и температуры в СИ |
|
Давление измеряют в Па, объем в м 3, температуру в К. |
Какое уравнение называют уравнением состояния? |
|
Уравнение, выражающее связь между макроскопическими параметрами состояния вещества, называется уравнением состояния этого вещества |
В чем заключается основная задача МКТ вещества? |
|
Основной задачей МКТ является нахождение уравнения состояния того или иного тел |
Какой вид имеет уравнение Менделеева-Клапейрона? |
|
|
Как формулируется закон Авогадро?
|
|
При одинаковых температурах и давлениях в равных объемах любых идеальных газов содержится одинаковое число молекул |
Сформулируйте закон Дальтона |
|
Давление смеси химически не взаимодействующих идеальных газов равно сумме парциальных давлений этих газов
|
Какое давление называют парциальным? |
|
Это давление, которое имел бы газ, входящий в состав газовой смеси, если бы он один занимал объем, равный объему смеси при той же температуре. |
В чем заключается объединенный газовый закон? |
|
Отношение произведения давления и объема идеального газа к его абсолютной температуре есть величина постоянная для данной массы данного газа. |
В каком виде объединенный газовый закон представил Клапейрон? |
|
|
Чему равна температура таяния льда и кипения воды при нормальном давлении по термодинамической шкале? |
|
Т л = 273 К Т в = 373 К |
Какой прибор служит для измерения давления газа? |
|
Манометр |
|
А теперь применим полученные уравнения при решении задач.
Слайд 23.
Обратите внимание:
Уравнение Менделеева-Клапейрона связывает между собой 5 физических величин, характеризующих состояние газа, — p, V, T, m, M – и позволяет по заданным четырем найти пятую величину.
Уравнение Менделеева-Клапейрона и все его следствия с большой точностью можно применить к газам, находящимся в условиях, близких к нормальным (t = 0 C, p = 1,013.105 Па), а также к разреженным газам.
Если плотность газа велика, а следовательно, взаимодействием молекул пренебречь нельзя, то модель идеального газа оказывается непригодной.
Проверьте, все ли величины выражены в СИ:
(1 л = 10-3 м3; 1 мм рт. ст. = 133 Па;
0 С = 273 К; нормальное атмосферное давление: 1,013.105 Па).
Учитывая эти советы, решить задачи:
(Слайд 24)
Сколько гелия потребуется для наполнения воздушного шара емкостью
500 м3 при нормальном атмосферном давлении и температуре300 К?
(Слайд 25)
Дано: Решение.
V = 500 м3 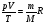 ,
,
p = 1,013.105 Па 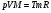 ,
,
Т = 300 К 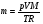 .
.
М = 4.10-3 кг/моль m = (1,013.105 Па . 500 м3.4.10-3 кг/моль)/
/300 К.8,31 Дж/(моль.К) = 81 кг.

Ответ: m = 81кг
m — ?
(Слайд 26)
Какова плотность сжатого воздуха при 0 С в камере шины автомобиля «Волга»? Давление 0,17 МПа.
(Слайд 27)
Дано: Решение.
Т=273 К рV/T=mR/M, где m=ρV,
р=0,17.106 Па pV/T=ρVR/M (сократим на V),
М=29.10-3 кг/моль p/T=ρR/M,
pM=TρR,
ρ=pM/TR,
ρ=(0,17.106.29.10-3) / (273.8,31)=2,17 кг/м3
ρ-? Ответ: 2,17 кг/м3
IV. Подведение итогов урока.
Сегодня мы с вами познакомились с основным уравнением состояния идеального газа и его следствиями. Но на этом изучение идеального газа не прекращается.
Подведение итогов работы обучающихся на уроке.
(Слайд 28)
V. Домашнее задание.
§ 68. Ответить на вопросы § 68
Упр. 13 (5,6).
