Губкинский район
Белгородская область
Урок по химии
«Почетный гражданин Белогорья – ЖЕЛЕЗО»
класс — 9
Учитель: Копцева Ирина Владимировна
с. Сапрыкино
Тема урока:
«Почетный гражданин Белогорья – ЖЕЛЕЗО»
Цели урока:
Обеспечить знание учащихся особенностей строения атомов металлов побочных подгрупп, физические и химические свойства простого вещества железа, области его применения.
Создать условия для развития умений составлять уравнения окислительно-восстановительных реакций, конспектировать, проводить химический эксперимент, делать выводы.
Воспитывать любовь к родному краю, бережное отношение к природе.
Тип урока: изучение нового материала.
Вид: Деловая игра.
Оборудование и материалы: коллекция «Полезных ископаемых», «Чугун и сталь», лозунги, магнит, портреты учёных, выставка книг по данной теме. Железо восстановленное, растворы соляной, серной кислот, сульфата меди (II), пробирки, штативы для пробирок, железный гвоздь, стакан.
Эпиграф:
Где бесновались «пантеры»,
«Тигры» сходили с ума,
Там распахнулись карьеры,
Железорудного КМА…. Ю. Грязнов.
Ход урока:
Организационный момент.
Изучение нового материала.
Секретарь (учащийся): Сегодня мы собрались для проведения расширенного заседания научного совета. Слово предоставляется председателю совета.
Председатель (учитель): На повестке дня у нас обсуждение одного вопроса о присвоении железу звания «Почётный гражданин Белгородчины». Почему именно железу мы предлагаем присудить его звание? (Вопрос задаётся классу, идёт обсуждение).
Ответ: Белгородская земля богата запасами железных руд. Прошу Вас коллеги вести подробнейший протокол обо всём, о чём здесь будет говориться. А я передаю слово химику.
Химик: Железо – это название химического элемента и знакомого металла: железный гвоздь, железная машина. Однако химический элемент железо есть не только там, но и в воде, в земле, в деревьях, в организме человека. Железо скапливается в болотах, отчего вода там иногда красноватая. А почему кровь красная? Догадались? Потому что в крови тоже есть частички железа. В организме человека его меньше напёрстка. Железо среди металлов занимает 2 место после алюминия.
Секретарь: Уважаемое «ЖЕЛЕЗО», просим Вас изложить кратко свою автобиографию.
ЖЕЛЕЗО (учащийся): Я проживаю и работаю на улице Менделеевской уже много сотен лет. Пусть обо мне расскажут мои коллеги. Что вам известно об элементе Железо? (обращается к классу, идёт обсуждение).
Положение в п. с.: 4 период VIII группа, побочная подгруппа.
Строение атома Ar (Fe) =56, Z+26)2 )8 )14 )2 P=26, e=26, n=30, 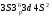
Возможно степени окисления: +2, +3, +6,0.
Соединение железа: оксиды, гидроксиды, соли.
ЖЕЛЕЗО: В отличие от изученных элементов валентные электроны находятся в атоме как на внешнем 4S подуровне, так и на предвнешнем 3d подуровне.
Появляются геологи (учащиеся) с рюкзаками за спиной.
Председатель научного совета: Постойте, постойте. А вы кто такие? (Поднимает рюкзак). Что это у вас здесь, камни что ли?
Геологи: Вы почти угадали. Мы геологи, путешествовали по всей стране, исследуя её подземные богатства. У нас в рюкзаках (показывает) полезные ископаемые – железные руды.
Геолог (учащийся №2): Вот это, например лимонит, им богат Крым (показывает по карте).
Геолог (учащийся №1): А это руда цвета живительной жидкости – крови, она так и называется гематит. От названия фермента крови – гемоглобина. Она была найдена нами на Украине. (Показывает по карте).
Геолог (учащийся №2): А это руда очень удивительная. Посмотрите, стрелка компаса в её присутствии отклоняется.
Геолог (учащийся №1): И это руда в огромных количествах встречается в Белгородской области, составляя запасы КМА.
Историк: Ещё в 1918 году в разгар гражданской войны, когда не утихали споры вокруг проблем и загадок магнитной аномалии, В.И. Ленин говорил:
“Мы имеем здесь почти, наверное, невиданные в мире богатства, которые способны перевернуть все дело металлургии”.
Ныне это действительно могучая кладовая подземных ископаемых, основная часть которых находиться на территории Белгородской области.
Краевед: Летом 1920 года президиум ВАСХНИЛ создал особую комиссию по изучению КМА, возглавили которую И.М. Губкин и его заместитель П.П. Лазарев. В августе 1931 г. принято решение заложить первую шахту КМА. Сейчас именем академика И.М. Губкина назван один из городов Белгородской области.
Председатель: Прошу секретаря представить нам характеристику простого вещества-железа.
Секретарь: (кратко о физических свойствах железа, его химической активности): характер мягкий, пластичный, общителен, притягивается магнитом, бел как снег, блестящая личность. (Демонстрирует образец железа, притяжение магнитом).
Председатель: Спасибо. А что же вы коллеги (обращается к учащимся класса) можете нам рассказать о химической активности железа (обсуждение фронтально на местах).
ЖЕЛЕЗО: Совершенно верно я очень дружу с кислородом, серой и другими металлами. Дружба наша носит окислительно-восстановительный характер.
Записи уравнений на доске и в тетради учащимся.
3Fe+202 → Fe+3203*Fe+2O
вос—ль ок—ль.
Fe+Se → Fe+2 S-2
Кислоты: Дайте и нам сказать доброе слово о железе. Мы его, ну просто обожаем. Из меня оно вытесняет взрывоопасный и зловредный водород /соляная кислота/
2H+1Cl+Fe0=Fe+2Cl-12+H2
ок- ль вос-ль
Со мною /серная кислота/ реагирует по-разному: когда я разбавленная, вытесняет водород, когда концентрированная действует по схеме:
Fe +H2 SO4→ SO2 + Fe2 (SO4) 3 + H2 O
Дома: электронный баланс коэффициенты.
ЖЕЛЕЗО:
Я дружу еще с некоторыми солями:
Я известно с давних пор и имею спрос
Опусти меня в раствор в медный купорос
Изменить хочу я соль, ну-ка выйди, соизволь.
Удивительный момент, стал другими раствор.
Вытесняя элемент, не вступаю в спор
На меня взгляни, ответь, начинаю я ржаветь (/класс дает ответ).
Fe +CuSO4→ Fe SO4 +Cu
Железо с водой при нагревании:
3Fe +4H+12O-2 → Fe+2O*Fe+32O3+4H2
Секретарь: Спасибо ЖЕЛЕЗО, просим МЕТАЛЛУРГА.
МЕТАЛЛУРГ: Железо можно получить в чистом виде восстановлением водородом, и алюминием из его оксидов, а также электролизом солей с валентностью железа (II).Чистое железо применяется для изготовления трансформаторов, но в основном его применяют в виде сплавов чугуна и стали /Демонстрирует сплавы /.
Краевед: Я хочу добавить, что сплавы железа бездоменным методом в электропечах выплавляют на Оскольском электрометаллургическом комбинате. Он является одним из ведущих предприятий черной металлургии России и единственным крупным комбинатом в нашей стране, работающим по технологии прямого восстановления железа.
Историк: комбинат расположен в непосредственной близости от месторождений высококачественных железных руд, входящих в состав Курской магнитной аномалии. Строительство комбината началось в 1978 году, первая промышленная продукция — окисленные железорудные окатыши — произведена в 1982 году. В 1983 году введена в эксплуатацию первая установка металлизации, в 1984 году – первые две электропечи.
Передовая технология производства, современное оборудование, высокая квалификация и богатый опыт рабочих, инженеров и управленцев комбината позволяет коллективу ОЭМК выпускать металл, пользующийся высоким спросом в России и за рубежом.
Секретарь: Вы приняли самое активное участие в обсуждении вопроса вынесенного на повестку дня. Просим вас заполнить листы для голосования. Чем больше правильных ответов, тем больше голосов в пользу железа (отвечают на тесты, самопроверка, собирают в конце урока).
Председатель: Наш научный совет подошел к концу. Большое спасибо всем за участие.
Подведение итогов урока. Выставление оценок.
Домашнее задание: изучить параграф 43, упр. №1-5, задача №1, подготовить презентацию (тема на выбор)
Сплавы железа, их многообразие и свойства
Физические свойства железа
Об истории открытия железа
Применение железа
Тестовое задание по теме: «Железо».
Тесовое задание по теме железо:
1. Железо находится в ____________ периоде, в ________ группе, ______ подгруппе.
2. Заряд ядра атома железа равен __________.
3. В атоме железа количество частиц:
а. 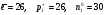
б. 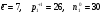
в. 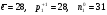
4. В атоме железа валентные электроны находятся:
а. 3S подуровни;
б. 4S подуровни;
в. 3D подуровни;
г. 4S b 3D подуровнях.
5. Строение атома железа
+7
а. 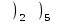
+26
б. 
+25
в. 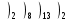
6. Железо в Белгородской области встречается в виде _________________.
7. Железо – это:
а. Газ без цвета и запаха;
б. Твердое вещество серебристо – белого цвета, притягивается магнитом;
в. Твердое вещество, желтого цвета.
8. Железо используют
а. В качестве топлива в быту и промышленности;
б. Как составная часть конструкционных материалов
в. Для изготовления трансформаторов
9. В химических реакциях железо проявляет свойства:
а. Окислителя и восстановителя
б. Восстановителя
в. Инертного вещества.
10. Железо реагирует:
а. С кислотами
б. Со щелочами
в. С солями
г. водой
11. Железо можно получить
а. Восстановлением железа из его окислов водородом, алюминием
б. При разложении солей при нагревании
в. Электролизом водных растворов солей без железа
12. Кто возглавил особую комиссию по изучению КМА:
б. Губкин
в. Курчатов
