9 класс
Химия
Тема: химические свойства растворов солей с точки зрения теории электролитической диссоциации
Цель: формировать представления об растворах солей используя теорию электролитической диссоциации
Задачи:
— рассмотреть и изучить особенности строения и свойств солей, их химическую активность.
— стимулировать познавательную активность ребят, развивать интерес к предмету, смекалку, эрудицию, умение быстро и четко формулировать и высказывать свои мысли, логически рассуждать.
— воспитывать чувство сопричастности общему делу, умение работать коллективно; воспитывать у учащихся трудолюбие, аккуратность и ответственность, любовь и интерес к предмету.
Методы и приемы: Словесный — объяснительно-иллюстративный, или информационно-рецептивный: рассказ.
Тип урока:
урок изучения и первичного закрепления новых знании.
Ход урока.
Организация деятельности учащихся
Актуализация ЗУН
Самостоятельная работа по теме «химические свойства растворов оснований с точки зрения ТЭД»
Изучение нового материала
Что такое соли в свете электролитической диссоциации?
Солями называют электролиты, которые при диссоциации образую катионы металлов и катионы аммония и анионы кислотных остатков.
Na2SO4 → 2 Na++SO42-
Классификация солей по составу
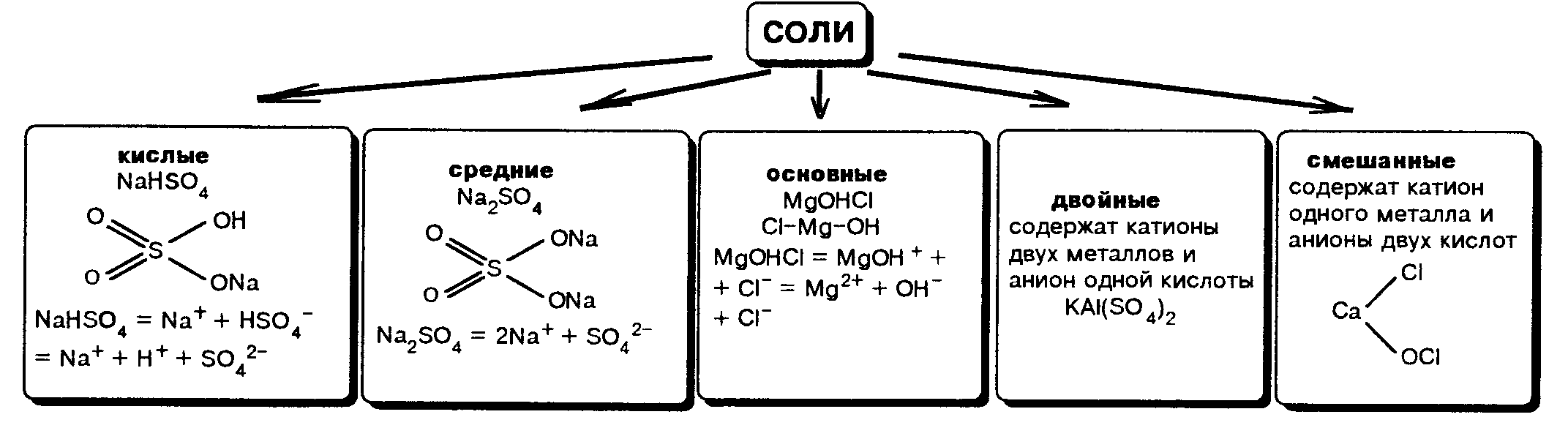
Применение солей
Многие соли применяют в быту (поваренная соль, сода), в качестве минеральных удобрений, при производстве стекла, моющих средств, взрывчатых веществ.
Таблица: «Химические свойства оснований в свете электролитической диссоциации».
| Химические свойства солей | Наблюдения и признаки реакций | Уравнения химических реакций | |
| 1 | Взаимодействие солей с металлами. I FeCl3 и Сu II CuSO4 и Fe III CuSO4 и Zn | I не реагирует II образуется медь III образуется медь | FeCl3 + Сu ≠ CuSO4 + Fe → FeSO4 + Cu CuSO4 + Zn → ZnSO4+Cu |
| 2 | Взаимодействие солей с растворами щелочей I NaOH и FeCl3 II КOH и СuSO4 III NaOH и | 1 – не идет реакция до конца 2, 3 – выпадают осадки | 3NaOH + FeCl3 → Fe(OH)3↓ +3 NaCl 3Na++3OH— + Fe3++3Cl — → Fe(OH)3↓ + 3 Na++3Cl— 3OH— + Fe3→ Fe(OH)3↓ 2КOH + СuSO4 → Cu(OH)2 ↓ + K2SO4 2К+<+2OH— + Сu2++SO4 2- → Cu(OH)2 ↓ + +2K+ +SO4 2- 2OH— + Сu2+→ Cu(OH)2 ↓ 2NaOH + Zn(NO3)2 → Zn(OH)2↓+2NaNO3 2Na++2OH— + Zn2++2NO3— → Zn(OH)2↓ + +2Na++2NO3 – 2OH— + Zn2+→ Zn(OH)2↓ |
| 3 | Взаимодействие солей с кислотами. Na2CO3 и HCl | Выделение газообразного вещества. | Na2CO3 +2 HCl → 2 NaCl + H2O + CO2↑ 2 Na+ + CO32- + 2H+ + 2Cl— → → 2 Na+ + 2Сl— + H2O CO32- +2H+→ H2O |
| 4 | Взаимодействие солей с солями I AgNO3 и NaCl II Na3PO4 и AgNO3 III BaCl2 и Na2SO4 | Выпадение различных осадков солей | AgNO3 + NaCl → AgCl ↓ + NaNO3 Ag++ NO3 — + Na+ + Cl— → AgCl ↓+ +Na+ +NO3 — Ag++ Cl— → AgCl ↓ 3AgNO3 + Na3PO4→ Ag3PO4 ↓ + 3KNO3 3Ag++3NO3 — + 3Na++ PO43 —→ Ag3PO4 ↓ + + 3Na++ NO3 — 3Ag++ PO43 —→ Ag3PO4 ↓ BaCl2 + Na2SO4 → BaSO4 ↓ + 2 NaCl Ba2++2Cl — + 2Na ++SO42- → BaSO4↓ + +2 Na+ + 2Cl— Ba2++SO42- → BaSO4 ↓ |
| 5 | Изменяют ли соли окраску индикаторов? АlCl3, NaCl, Na2CO3 | Изменяют, но не все |
|
Закрепление
особенности строения солей
характеристика химических свойств солей – примеры.
Д/з
