



КАЛИНИНГРАДСКИЙ ТОРГОВО-ЭКОНОМИЧЕСКИЙ КОЛЛЕДЖ 
филиал федерального государственного бюджетного
образовательного учреждения высшего профессионального образования
РОССИЙСКАЯ АКАДЕМИЯ НАРОДНОГО ХОЗЯЙСТВА и ГОСУДАРСТВЕННОЙ СЛУЖБЫ
при ПРЕЗИДЕНТЕ РОССИЙСКОЙ ФЕДЕРАЦИИ
Опорный конспект
Тема: «Дисперсные системы»
Калининград, 2013
Тема: «Дисперсные системы»
Дисперсные системы – системы, состоящие из множества малых частиц, распределенных в жидкой, твердой или газообразной среде.
Дисперсная система включает в себя два обязательных компонента – это
дисперсная фаза — измельченное вещество
дисперсионная среда – вещество, в котором распределена дисперсная фаза.
Для всех дисперсных систем характерны два основных признака:
Высокая дисперсность.
Гетерогенность.
Дисперсные системы
Тонко дисперсные Коллоидные системы Грубо дсперсные
Суспензии Золи Истинные
Эмульсии Гели
Аэрозоли
Пены
порошки
Классификация дисперсных систем
По агрегатному состоянию фаз
И дисперсионную среду, и дисперсную фазу могут представлять вещества, находящиеся в различных агрегатных состояниях — твердом, жидком и газообразном.
В зависимости от сочетания агрегатного состояния дисперсионной среды и дисперсной фазы можно выделить 9 видов таких систем.
Основные типы дисперсных систем
| Дисперсная фаза | |||
| Газ | Жидкость | Твердое тело | |
| Газ | Дисперсная система не существует | Аэрозоли (туман, облака, аэрозоли жидких лекарств, духов) | Аэрозоли (дым, пыль, песчаные бури) |
| Жидкость | Жидкие пены, газовые эмульсии | Эмульсии (сливочное масло, кремы, мази, пищеварительные соки) | Суспензии и коллоидные растворы (кисели, студни, соусы, клеи) |
| Твердое тело | Твердые пены (хлеб, пемза, пенопласты, шоколад) | Жемчуг, капиллярные системы | Сплавы |
По размеру частиц
По степени дисперсности системы распределяют на типы
Грубодисперсные с радиусом частиц более 100 нм
Коллоидно-дисперсные (золи) с размером частиц 100 нм до 1 нм.
Молекулярные или ионные растворы с размером частиц менее 1 нм.
Грубодисперсные системы.
Эмульсии (и среда, и фаза — нерастворимые друг в друге жидкости, в которых одна из жидкостей взвешена в другой в виде капелек). Это молоко, лимфа, водоэмульсионные краски , сметана, майонез, мороженное.и т. д.;
Суспензии (среда — жидкость, а фаза — нерастворимое в ней твердое вещество). Это строительные растворы (например, «известковое молоко» для побелки), взвешенный в воде речной и морской ил, протертый суп.
Аэрозоли — дисперсные системы, дисперсионной средой которых является газ, а дисперсной фазой могут быть твердые частицы или капельки жидкости. Различают пыли, дымы, туманы. Первые два вида аэрозолей представляют собой взвеси твердых частиц в газе (более крупные частицы в пылях), последний — взвесь мелких капелек жидкости в газе. Биоаэрозоли – пыльца и споры растений.
Пены — высококонцентрированные грубодисперсные системы, в которых дисперсионная среда жидкость, а дисперсная фаза газ.
Порошки – дисперсная фаза – твердое вещество, а дисперсионная среде – газ.
Грубодисперсные системы неустойчивы.
Коллоидные системы
Коллоидные системы — это такие дисперсные системы, в которых размер частиц фазы от 100 до 1 нм. Эти частицы не видны невооруженным глазом, и дисперсная фаза и дисперсионная среда в таких системах отстаиванием разделяются с трудом.
Их подразделяют на золи (коллоидные растворы) и гели (студни).
1. Коллоидные растворы, или золи. Это большинство жидкостей живой клетки (цитоплазма, ядерный сок , содержимое органоидов и вакуолей) и живого организма в целом (кровь, лимфа, тканевая жидкость, пищеварительные соки). Такие системы образуют клеи, крахмал, белки, некоторые полимеры.
Коллоидные растворы внешне похожи на истинные растворы. Их отличают от последних по образующейся «светящейся дорожке» — конусу при пропускании через них луча света.
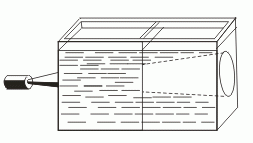
Это явление называют эффектом Тиндаля. Более крупные, чем в истинном растворе, частицы дисперсной фазы золя отражают свет от своей поверхности, и наблюдатель видит в сосуде с коллоидным раствором светящийся конус. В истинном растворе он не образуется. Аналогичный эффект, но только для аэрозольного, а не жидкого коллоида, вы можете наблюдать в кинотеатрах при прохождении луча света от киноаппарата через воздух кинозала.
Частицы дисперсной фазы коллоидных растворов нередко не оседают даже при длительном хранении из-за непрерывных соударений с молекулами растворителя за счет теплового движения. Они не слипаются и при сближении друг с другом из-за наличия на их поверхности одноименных электрических зарядов. Но при определенных условиях может происходить процесс коагуляции.
Коагуляция — явление слипания коллоидных частиц и выпадения их в осадок — наблюдается при нейтрализации зарядов этих частиц, когда в коллоидный раствор добавляют электролит. При этом раствор превращается в суспензию или гель. Некоторые органические коллоиды коагулируют при нагревании (клей, яичный белок) или при изменении кислотно-щелочной среды раствора.
2. Гели, или студни, представляющие собой студенистые осадки, образующиеся при коагуляции золей. К ним относят большое количество полимерных гелей, столь хорошо известные вам кондитерские, косметические и медицинские гели (желатин, холодец, желе, мармелад, торт «Птичье молоко») и конечно же бесконечное множество природных гелей: минералы (опал), тела медуз, хрящи, сухожилия, волосы, мышечная и нервная ткани и т. д. Со временем структура гелей нарушается — из них выделяется вода. Это явление называют синерезисом.
Растворы
Раствор — гомогенная (однородная) система, состоящая из частиц растворенного вещества, растворителя и продуктов их взаимодействия
Растворы всегда однофазны, то есть представляют собой однородный газ, жидкость или твердое вещество. Это связано с тем, что одно из веществ распределено в массе другого в виде молекул, атомов или ионов (размер частиц менее 1 нм). Растворы называют истинными, если требуется подчеркнуть их отличие от коллоидных растворов.
Таблица
Примеры дисперсных систем
| Дисперсионная фаза | Примеры некоторых природных и бытовых дисперсных систем | |
| Газ | Газ Жидкость Твердое вещество | Всегда гомогенная смесь (воздух, природный газ) Туман, попутный газ с капельками нефти, карбюраторная смесь в двигателях автомобилей (капельки бензина в воздухе), аэрозоли Пыли в воздухе, дымы, смог, самумы (пыльные и песчаные бури), аэрозоли |
| Жидкость | Газ Жидкость Твердое вещество | Шипучие напитки, пены Эмульсии. Жидкие среды организма (плазма крови, лимфа, пищеварительные соки), жидкое содержимое клеток (цитоплазма, кариоплазма) Золи, гели, пасты (кисели, студни, клеи). Речной и морской ил, взвешенные в воде; строительные растворы |
| Твердое вещество | Газ Жидкость Твердое вещество | Снежный наст с пузырьками воздуха в нем, почва, текстильные ткани, кирпич и керамика, поролон, пористый шоколад, порошки Влажная почва, медицинские и косметические средства (мази, тушь, помада и т. д.) Горные породы, цветные стекла, некоторые сплавы |
Вопросы для самопроверки
Что называется дисперсной системой, фазой, средой?
Как связать дисперсность с размером частиц?
Какие дисперсные системы относятся к коллоидным?
Что такое коагуляция и какие факторы ее вызывают?
Каково практическое значение коагуляции?
Что называется суспензией?
Каковы основные свойства суспензий?
Что такое эмульсия и как можно ее разрушить ?
Где применяютя аэрозоли?
Какие существуют способы разрушения аэрозолей?
Техника безопасности при работе со спиртовками
При работе со спиртовками надо соблюдать правила техники безопасности.
Необходимо использовать спиртовку только по назначению, указанному в ее техническом паспорте.
Запрещается заправлять спиртовку вблизи устройств с открытым пламенем.
Не заполнять спиртовку топливом более чем наполовину объема резервуара.
Нельзя перемещать или переносить спиртовку с горящим фитилем.
Категорически запрещается зажигать фитиль спиртовки посредством другой спиртовки.
Заправлять спиртовку только этиловым спиртом.
Гасить пламя спиртовки только посредством колпачка.
Не держать на рабочем столе, где используется спиртовка, легковоспламеняющиеся вещества и материалы, способные воспламеняться от кратковременного воздействия источника зажигания с низкой тепловой энергией (пламя спички,спиртовки).
При работе не наклонять спиртовку, а при возникновении такой необходимости, использовать спиртовки, работающие в наклонном положении ( граненые спиртовки ).
При опрокидывании спиртовки и разливе на столе горящего спирта немедленно накройте спиртовку плотной тканью, а при необходимости используйте для гашения пламени и огнетушитель.
Помещение в котором производится работа со спиртовкой (спиртовками) должно быть оснащено первичными средствами пожаротушения, например, порошковым огнетушителем марки ОП-1 или ОП-2.
Литература
А.Д. Зимон «Занимательная коллоидная химия», Москва, «Агар, 2008 г.
Н.А. Жарких «Химия для экономических колледжей», Ростов – на Дону, «Феникс», 2008 г
Физическая и коллоидная химия в общественном питании, Москва, Альфа — М 2010.
Э.А. Арустамов «Природопользование», Москва, «Дашков и К»,2008.
https://ru.wikipedia.org
https://festival.1september.ru/articles/575855/
2
