Бондаренко Ирина Николаевна, учитель биологии и географии
Позднякова Татьяна Степановна, учитель химии
Муниципального общеобразовательного учреждения Усвятская средняя общеобразовательная школа Дорогобужского района Смоленской области
Номинация: Естественные науки
Название работы: «Изучение экологического состояния родника»
Муниципальное общеобразовательное учреждение
Усвятская средняя общеобразовательная школа
Дорогобужского района Смоленской области
НАУЧНО – ИССЛЕДОВАТЕЛЬСКАЯ РАБОТА


ученика 11 класса Бурдакова Кирилла
Руководители: учитель биологии Бондаренко И.Н.
учитель химии Позднякова Т.С.
Усвятье
2009 год
ПЛАН
Актуальность
Методика проведения исследований.
Общая географическая и геологическая характеристика района родника.
Характеристика растительного и животного мира.
Исследования родника:
а) историческая справка;
б) характеристика физико-химических свойств воды родника.
Заключение.
Литература.
1. Актуальность
Вода — одно из самых необходимых веществ для жизни всего живого. Она представлена в природе в виде поверхностных и подземных вод. В настоящее время в результате бурного развития технического прогресса и более интенсивного загрязнения окружающей среды предъявляются новые требования к качеству воды. Становится необходимостью строительство новых водохранилищ и водозаборов из рек. А наши предки для питьевых нужд пользовались в основном подземными «жилами», то есть колодцами и родниками. И сейчас этими источниками можно пользоваться, особенно в случае загрязнения воды в поверхностных водоёмах.
Вода подземных источников обладает следующими достоинствами: биологически стерильна, изолирована от попадания промышленных стоков. Изучив народные приёмы пользования подземных вод, обогатив их методами современной науки и техники, можно успешно решать проблемы обеспечения питьевой водой не только сельского, но и городского населения.
Вода, содержащаяся в породах земной коры, называется подземной. Подземные воды участвуют в большом круговороте воды. Происходит постоянный водообмен между гидросферой, атмосферой, литосферой и биосферой Земли. При неглубоком залегании она попадает в атмосферу в виде пара, исходящего от земли. Это явление хорошо заметно по лёгкому мареву, возникающему над её поверхностью в жаркие летние дни.
Другой путь вовлечения подземной влаги в великий круговорот воды происходит на участках её выхода на поверхность, и чаще всего — в понижениях рельефа, где процессы разлива (эрозии) вскрывают водоносные слои. Подземные воды на таких участках переходят в поверхностные многочисленные родники, пополняя запасы вод в реках, морях и океанах.
Происхождение подземных вод различно. При просачивании (инфильтрации) в грунт дождевой и талой воды, а также при фильтрации из поверхностных водоёмов образуются так называемые инфильтрационные подземные воды, являющиеся золотым фондом человечества, так как именно они формируют зону пресных вод, месторождения которых используются в водоснабжении. Выходы подземных вод на дневную поверхность образуют родники.
По характеру выхода различают родники нисходящие и восходящие. Первые образуются при разгрузке грунтовых или межпластовых слабо напорных вод, а вторые — напорных. Вода восходящих родников часто имеет повышенную минерализацию, так как путь её длиннее, чем у родников, питающихся безнапорными водами и выход их более бурный, чем у последних.
В последнее время в России возрождаются идеи чуткого и бережного отношения к природным объектам, в том числе и к родникам вследствие возрастания числа экологических проблем. В настоящее время изучение родников представляет большой научный и практический интерес.
Крупные родники довольно редкое явление. Расположенные вблизи населённых пунктов, они, как правило, представляют историческую ценность, поскольку в ранний исторический период часто определяли место будущего поселения. Таким примером служит родник у деревни Усвятье. Первые, наиболее древние поселения обнаружены как раз на этом участке территории.
Основой работ по исследованию данного родника стало то, что в 2007 году ученики МОУ Усвятская средняя общеобразовательная школа в рамках природоохранной деятельности реализовали социальный проект «Живи, Святой ручей!», получивший широкое общественное признание.
 В ходе реализации проекта был благоустроен сам родник и прилежащая к нему территория, намечен план работ по сохранению родника как исторической и географической достопримечательности. Советом старшеклассников одобрена идея дальнейшего его изучения.
В ходе реализации проекта был благоустроен сам родник и прилежащая к нему территория, намечен план работ по сохранению родника как исторической и географической достопримечательности. Советом старшеклассников одобрена идея дальнейшего его изучения.
Членами химико-экологического кружка Усвятской средней общеобразовательной школы исследован сам родник, бактериологический и физико-химический состав воды из родника. Они определяли: органолептические показатели — вкус, запах, цветность, прозрачность, а также общую жесткость, водородный показатель рН, общее железо, сульфаты, хлориды, азот и аммиак.

Исследования, которые невозможно было провести в условиях школьной лаборатории, были проведены в химической лаборатории санитарно-эпидемиологической службы.
Цели проведенных исследований:
1). Изучение экологического состояния родника и прилегающей территории, проведение микробиологического и физико-химического анализа воды.
2). Подтверждение гипотезы об исключительной чистоте родниковой воды.
Издавна среди населения бытует мнение, что все родниковые воды являются исключительно чистыми и пригодными к употреблению без всяких ограничений. В связи с этим возникла необходимость выяснить, так ли это на самом деле?
Задачи:
— взять пробы воды из родника, реки Ужа, водопровода;
— провести физико-химический анализ проб;
— сравнить полученные результаты с пробами воды из водопровода и из реки Ужа;
— выявить различия и объяснить их причины;
— констатировать данные по микробиологическому анализу родниковой воды, проведённому в лаборатории санитарно- эпидемиологической службы.

2. Методика проведения исследований.
С целью изучения родника были организованы несколько экспедиций. Составлен паспорт родника, в который занесены все основные сведения об источнике: местонахождение, географические условия выхода, характер выхода на поверхность земли, влияние на окружающую местность, хозяйственно- бытовое использование, а также данные физико-химического анализа и краеведческие сведения.
Отбор проб проводился по следующим правилам: использовалась только стеклянная посуда, тщательно промытая и ополоснутая дистиллированной водой; сосуды закрывались притертыми пробками; поверхностные пробы брались прямо в сосуд. Для получения достоверных результатов анализ проводился не позднее 1,5 часов после их отбора, чтобы вода не успела претерпеть нежелательных изменений.
 В исследуемых водных источниках были взяты пробы воды и выполнен физико-химический анализ по основным параметрам. Работы проводились по стандартным методикам.
В исследуемых водных источниках были взяты пробы воды и выполнен физико-химический анализ по основным параметрам. Работы проводились по стандартным методикам.
Методика анализа проб воды.
| ПДК | Реактивы | Лабораторное оборудование | |
| Определение рН | 6,0-8,0 | Универсальный индикатор | Пробирки, бюретки |
| Определение окисляемости | 4-8 мг О/л | Серная кислота (1:3) 0,01 н.р-р перманганата калия | Колба, бюретки |
| Определение аммонийного азота | До2,5 мг/л | Реактив Неслера, хлорид ртути(II), дистиллированная вода, йодид калия, гидроксид натрия | Пробирки, хим. стакан, газовая горелка, колба, фильтровальная бумага |
| Определение нитритов | 0,002 мг/л | Дистиллированная вода, активированный уголь, хлорид алюминия, реактив Грисса | Пробирки, хим. стакан |
| Определение нитратов | 10 мг/л | 10% хлорид натрия 0,005 р-р дифениламина | Пипетки, хим. стакан |
| Определение сульфатов | 400 мг/л | Р-р соляной кислоты(1:5) 5% хлорид бария | Пипетки, хим. стакан |
| Определение фосфатов | До 0,1мг/л | Магнезиальная смесь | Пипетки, хим. стакан |
| Определение железа общего | 0,3 мг/л | Концентрированная азотная кислота, р-р пероксида водорода, р-р роданида калия | Пипетки, хим. стакан |
| Определение 6имхлорида | 350 мг/л | 10% р-р нитрата серебра | Пипетки, хим. стакан |
| Определение жесткости | 7.0-10,0 Моль экв/л | Аммиачный буферный р-р, черный эриохром Т, трилон Б | Пипетки, колба |
Более подробно методики анализа проб воды описаны в приложении (приложение 1).
Для получения исторических и краеведческих сведений проведены беседы с местными жителями, работниками городского и школьного музеев.

3. Общая географическая и геологическая характеристика
района Святого ручья.
Родник расположен в 2 км на юго-запад от деревни Усвятье в отрицательной замкнутой форме рельефа – балке, её ширина – 30м, глубина – 10м. Балка расположена в пойменном комплексе на первой надпойменной террасе реки Ужа и представляет собой водно-эррозиционную форму рельефа.
Территория, по которой протекает Святой ручей, сложена породами каменноугольной системы Видейского яруса, яснополянского надгоризонья и представлена известняками, глиной и песками. Четвертичные породы представлены аллювиальными отложениями.
4. Характеристика растительности и животного мира.
Склоны балки заросли мелколиственными породами деревьев: берёзой, ольхой, осиной, черёмухой. Растительность на дне балки характерна для увлажненных мест. Здесь растут папоротники, крапива, щавель, калужница, василистник водосбористый, осока острая. Животный мир вокруг родника представлен различными птицами, встречаются лягушка остромордая, жаба серая.
5. Исследование родника.
а). Историческая справка о происхождении названия родника.
О месте, где сейчас располагается родник, сложены легенды. Вот одна из них:
давным-давно выше по склону стояла церковь. Подземные ключи подмыли её берега, и она ушла под воду. На этом месте образовалось небольшое озеро. Если нырнуть в него, то невозможно достать дна, зато можно услышать звон колоколов. Из этого озера и взял своё начало Святой ручей.
Название деревни – Усвятье, по преданию тоже произошло от Святого ручья
( у- святого). Ещё недавно родник представлял собой неприглядное зрелище, так как на его берегах была устроена свалка. И только усилиями учеников школы и жителей деревни в ходе реализации социального проекта «Живи, Святой ручей!» удалось привести в порядок это историческое место.
Многие жители деревни хотят видеть родник ухоженным, поэтому жителям деревни необходимо следить за порядком у родника и за сохранностью лавочек и дощатых мостков возле Святого ручья.
Это свидетельствует о том, что жители деревни очень любят свою достопримечательность и хотят заботиться о ней. Мною обобщены результаты социологического опроса жителей деревни Усвятье:
— 94% опрошенных жителей деревни Усвятье периодически посещает родник;
— 94% верят в целебную силу родниковой воды;
— 100% считают источник достопримечательностью Усвятского сельского поселения;
— 98% высказали мнение, что территорию около родника необходимо благоустраивать и поддерживать в надлежащем состоянии;
— 83% готовы участвовать в благоустройстве.
Таким образом: у родника богатая история, родник является достопримечательностью Усвятского сельского поселения и не только; живо культурное наследие родника.
б). Характеристика физико-химических свойств воды родника.
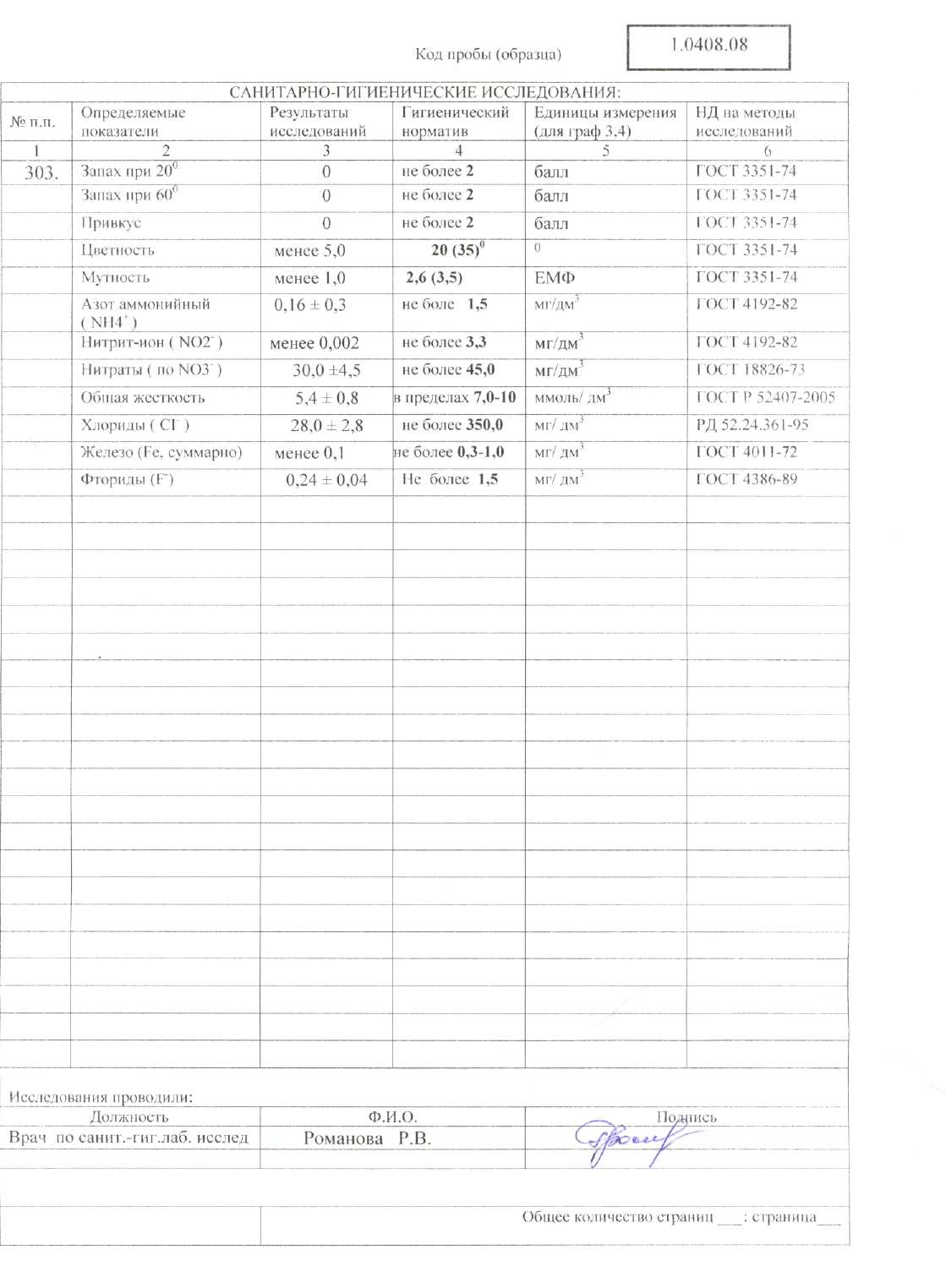
Воду из родника пьют, а также ей омываются. Химический анализ части проб воды был проведён силами химико-экологического кружка, другой части проб — СЭС. Полученные в ходе моих исследований данные незначительно отличаются от аналогичных исследований СЭС.
Они представлены в таблице (приложение 2).
На основании полученных данных можно сделать вывод о том, что вода родника соответствует нормам качества питьевой воды.
Для сравнения были проведены анализы воды из водопровода в школе (приложение 3), а также из реки Ужа (приложение 4). Сравнительный анализ этих проб показывает, что родниковая вода по своим физико-химическим свойствам и органолептическим показателям превосходит водопроводную.
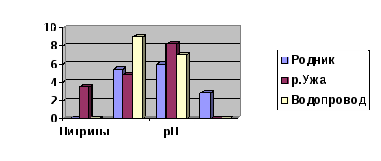

Воду из реки для питья использовать нельзя, так как в ней превышено содержание азота, нитритов и нитратов, что не соответствует санитарно-гигиеническим нормам. Высокое содержание этих веществ можно объяснить тем, что в воду попадают стоки животноводческих ферм и удобрения с полей.
6. Заключение
Согласно Всеобщей декларации прав человека право на чистую воду, ее охрану и информацию о качестве воды — основные права человека, защищающие не только его здоровье, но и жизнь. Россия занимает первое место в мире по запасам пресных вод — здесь сосредоточено более 20 % мировых ресурсов. Речной сток составляет 4270 км3 в год (10 % мирового речного стока), т. е. по 30 тыс. м3 воды на каждого жителя. В озерах сосредоточено более 26 тыс. км3 пресных вод. Разведанные запасы подземных вод позволяют использовать от 30 до 300 км3 в год. Кроме того, в России действуют более 2000 водохранилищ объемом более 1 млн. м3 каждое и 37 крупных систем межбассейнового перераспределения стока. Тем не менее, проблема загрязнения водоемов и нехватки питьевой воды в России одна из самых актуальных.
Мировые запасы пресной воды не увеличиваются, а ее потребление постоянно растет. В связи с этим 22 февраля 1993 г. Генеральная Ассамблея организации Объединенных Наций объявила 22 марта Всемирным днем воды (водных ресурсов). Цель этого праздника — привлечь внимание к проблемам нехватки питьевой воды, необходимости сохранения и рационального использования водных ресурсов. К проведению Всемирного дня воды привлекаются правительства разных государств, международные агентства, общественные организации, учреждения образования и культуры. Каждый человек должен сделать все возможное для сохранения и улучшения качества пресной воды, увеличения ее количества для будущих поколений.
Я в своей работе обобщил исследования воды из родника, который является исторической и географической достопримечательностью Усвятского сельского поселения. В ходе исследований:
Составлен паспорт Родника.
Установлено происхождение Родника.
Изучено его культурное наследие.
Определен физико-химический состав родниковой воды.
В результате проведённых исследований поставленные цели достигнуты, задачи выполнены.
Литература
1. Эстрин «Методическое пособие по химико-физическому анализу воды»,
Москва 1996 г.
2. Природа Смоленской области» под ред. М.А.Шкаликова, Смоленск, 2001 г.

Название по карте: Святой ручей
Местоположение: Родник расположен в 2 км на юго-запад от деревни Усвятье.
Подъезды (подходы): просёлочная дорога от д. Усвятье
Геологические условия выхода воды
*характеристика пласта, из которого вытекает подземная вода: песчаный.
* породы водоупорного пласта: глина.
*характер истечения: выходит из стенки берега
* расстояние источника от уреза реки: 300-400м.
5. Растительность вблизи родника: ольха, осина, берёза, малина, папоротник, осока,
6. Животный мир вокруг родника: различные птицы, лягушка остромордая, жаба серая.
7. Физические особенности воды в роднике
* цветность: прозрачная
* запах: отсутствует
*привкус: 0 баллов
* осадок: отсутствует, железо не обнаружено.
* замерзание: не замерзает
* дебит источника: подземные воды
8. химические свойства воды: рН=6.0, присутствуют сульфиды, хлориды,
8. Влияние родника на окружающую местность: воды родника способствуют заболачиванию территории, в результате смыкания поверхностных и подземных вод. Признаками заболоченности являются увлажнения почвы, непересыхающие даже летом и наличие растений-индикаторов.
9. Определение мощности родника: банка ёмкостью 1л заполнилась за 20с, за час – 180л, за сутки – 4320л.
10. Зависимость количества воды в роднике от погоды: после обильных дождей и таяния снега количество в роднике увеличивается.
11. Куда течет вода из родника: вода родника образует ручей, впадающий в болото.
12.Хозяйственное использование родника: вода родника имеет ритуальное значение.
13 Благоустройство родника: силами учащихся Усвятской школы был сделан деревянный сруб вокруг родника и благоустроена территория около ручья
14 Предложения по охране и рациональному использованию родника: продолжать уход за родником и прекратить выпас скота вблизи ручья.
15. Кто составил паспорт: Бурдаков Кирилл.
16. Дата заполнения: 7. 03. 09.
Приложение 1
ИССЛЕДОВАНИЕ КАЧЕСТВА ПИТЬЕВОЙ ВОДЫ
Органолептические показатели воды
1. Содержание взвешенных частиц
Этот показатель качества воды определяют фильтрованием определенного объема воды через бумажный фильтр и последующим высушиванием осадка на фильтре в сушильном шкафу до постоянной массы. Для анализа берут 500-1000 мл воды. Фильтр перед работой взвешивают. После фильтрования осадок с фильтром высушивают до постоянной массы при 105 «С, охлаждают взвешивают. Весы должны обладать высокой чувствительностью, лучше использовать аналитические весы.
Содержание взвешенных веществ в мг/л в испытуемой воде определяют по формуле
(тг — т2) • 1000/К
где Wj — масса бумажного фильтра с осадком взвешенных частиц, г; т2 — масса бумажного фильтра до опыта, г; V — объем воды для анализа, л. ПДК = 10 мг/л.
2. Цвет (окраска)
При загрязнении водоема стоками промышленных предприятий вода может иметь окраску, не свойственную цветности природных вод. Для источников хозяйственно-питьевого водоснабжения окраска не должна обнаруживаться в столбике высотой 20 см, для водоемов культурно-бытового назначения — 10 см.
Диагностика цвета — один из показателей состояния водоема. Для определения цветности воды нужны стеклянный сосуд и лист белой бумаги. В сосуд набирают воду и на белом фоне бумаги определяют цвет воды (голубой, зеленый, серый, желтый, коричневый) — показатель определенного вида загрязнения.
3. Прозрачность
Прозрачность воды зависит от нескольких факторов: количества взвешенных частиц ила, глины, песка, микроорганизмов, содержания химических соединений.
Для определения прозрачности воды используют прозрачный мерный цилиндр с плоским дном, в который наливают воду, подкладывают под цилиндр на расстоянии 4 см от его дна шрифт, высота букв которого 2 мм, а толщина линий букв — 0,5 мм, и сливают воду до тех пор, пока сверху через слой воды не будет виден этот шрифт. Измеряют высоту столба оставшейся воды линейкой и выражают степень прозрачности в е сантиметрах. При прозрачности воды менее 3 см водопотребление ограничивается. Уменьшение прозрачности природных вод свидетельствует об их загрязнении.
4. Запах
Запах воды обусловлен наличием в ней пахнущих веществ, которые попадают в нее
естественным путем и со сточными водами.
Запах воды водоемов, обнаруживаемый непосредственно в воде или (водоемов хозяйственно-питьевого назначения) после ее 1 хлорирования, не должен превышать 2 баллов. Определение основано на органолептическом исследовании характера и интенсивности запахов воды при 20 и 60 °С. Характер и интенсивность запаха определяют по предлагаемой методике (табл. 2, 3).
Запахи искусственного происхождения (от промышленных выбросов, для питьевой воды — от обработки воды реагентами на водопроводных сооружениях и т. п.) называются по соответствующим веществам: хлорфенольный, камфорный, бензиноиый, хлорный и т. п.
Интенсивность запаха также оценивается при 20 и 60 «С по 5-балльной системе согласно таблице.
Запах воды следует определять в помещении, в котором воздух не имеет постороннего запаха. Желательно, чтобы характер и интенсивность запаха отмечали несколько исследователей.
|
| ||||
| Характер запаха | Примерный род запаха |
| ||
| Ароматический | Огуречный, цветочный |
| ||
| Болотный | Илистый, тинистый |
| ||
| Шилостный | Фекальный, сточной воды |
| ||
| Древесный | Мокрой щепы, древесной коры |
| ||
| Землистый | Прелый, свежевспаханной земли, глинистый |
| ||
| Плесневый | Затхлый, застойный |
| ||
| Рыбный | Рыбы, рыбьего жира |
| ||
| Сероводородный | Тухлых яиц |
| ||
| Травянистый | Скошенной травы, сена |
| ||
| Неопределенный | Не подходящий под предыдущие определения |
| ||
|
| ||||
| Балл | Интенсивность запаха | Качественная характеристика | ||
| — | Отсутствие ощутимого запаха | |||
| 1 | Очень слабая | Запах, не поддающийся обнаружению потребителем, но обнаруживаемый в лаборатории опытным исследователем | ||
| 2 | Слабая | Запах, не привлекающей внимания потребителя, но обнаруживаемый, если на него обратить внимание | ||
| 3 | Заметная | Запах, легко обнаруживаемый и дающий повод относиться к воде с неодобрением | ||
Определение качества воды методами химического анализа
Водородный показатель (рН)
Питьевая вода должна иметь нейтральную реакцию (рН около 7). Значение рН воды водоемов хозяйственного, питьевого, культурно-бытового назначения регламентируется в пределах 6,5-8,5.
Оценивать значение рН можно разными способами.
1.Приближенное значение рН определяют следующим образом. В пробирку наливают 5 мл исследуемой воды, 0,1 мл универсального индикатора, перемешивают и по окраске раствора определяют рН:
• розово-оранжевая — рН около 5;
• светло-желтая — 6;
• зеленовато-голубая — 8.
2.Можно определить рН с помощью универсальной индикаторной бумаги, сравнивая ее окраску со шкалой.
3. Наиболее точно значение рН можно определить на рН-метре или по шкале набора Алямовского.
Жесткость воды
Различают общую, временную и постоянную жесткость воды. Общая жесткость обусловлена главным образом присутствием растворимых соединений кальция и магния в воде. Временная жесткость иначе называется устранимой или карбонатной. Она обусловлена наличием гидрокарбонатов кальция и магния. Постоянная (некарбонатная) жесткость вызвана присутствием других растворимых солей кальция и магния.
Общая жесткость варьирует в широких пределах в зависимости от типа пород и почв, слагающих бассейн водосбора, а также от сезона года. Значение общей жесткости в источниках централизованного водоснабжения допускается до 7 ммоль • экв./л, в отдельных случаях по согласованию с органами санитарно-эпидемиологической службы — до 10 ммоль • экв./л. При жесткости до 4 ммоль • экв./л вода считается мягкой, 4-8 ммоль • экв./л — средней жесткости, 8-12 ммоль • экв./л — жесткой, более 12 ммоль • экв./л — очень жесткой.
Методами химического анализа обычно определяют жесткость общую (Ж*,) и карбонатную (Жк), а некарбонатную (Жн) рассчитывают как разность Жо — Жк.
Определение карбонатной жесткости воды
Расчет концентраций карбонат- и гидрокарбонат-ионов
В склянку наливают 10 мл анализируемой воды, добавляют 5-6 капель фенолфталеина. Если при этом окраска не появляется, то считается, что карбонат-ионы в пробе отсутствуют. В случае возникновения розовой окраски пробу титруют 0,05 н. раствором соляной кислоты до обесцвечивания. Концентрацию карбонат-ионов рассчитывают по формуле
Ск= К(НС1)-О,О5-6О-1ООО=у(нс1).ЗОО)
где ск — концентрация карбонат-иона, мг/л; 7(НС1) — объем соляной кислоты, израсходованной на титрование, мл. Затем в той же пробе определяют концентрацию гидрокарбонат-ионов. К пробе доба-вить 1-2 капли метилового оранжевого. При этом проба приобретает желтую окраску. Титруют пробу раствором 0,05 н. соляной кислоты до перехода желтой окраски в розовую. Концентрацию гидрокарбонат-ионов рассчитывают по формуле Сгк=К(НС1)- 0,05 -61 • Ю00 =7(нс1). 305, где сге — концентрация гидрокарбонат-иона, мг/л; 7(НС1) — объем соляной кислоты, израсходованной на титрование, мл.
Карбонатную жесткость Жк рассчитывают, суммируя значения концентраций карбонат- и гидрокарбонат-ионов по формуле Жк = ск— 0,0333 + сга-0,0164,
где 0,0333 и 0,0164 — коэффициенты, равные значениям, обратным эквивалентным массам этих анионов.
Определение аммиака и ионов аммония
Определение аммиака и ионов аммония (качественное с приближенной количественной оценкой). Предельно допустимая концентрация (ПДК) аммиака и ионов аммония в воде водоемов 2 мг/л по азоту или 2,6 мг/л в виде иона аммония.
В пробирку диаметром 13-14 мм наливают 10 мл исследуемой воды, прибавляют 0,2-0,3 мл 30 %-ного раствора сегнетовой соли и 0,2 мл реактива Неслера. Через 10-15 мин проводят приближенное определение по табл. 4.
Определение нитратов и нитритов
Предельно допустимая концентрация (ПДК) нитритов (Шг) в питьевой воде водоемов составляет 3,3 мг/л, нитратов (Шз) -45 мг/л.
На часовое или предметное стекло помещают три капли раствора дифениламина, приготовленного на концентрированной серной кислоте, и одну-две капли исследуемой воды. В присутствии нитрат- и нитрит-ионов появляется синее окрашивание, интенсивность которого зависит от их концентрации.
|
|
|
| |
| Ориентировочное суммарное содержание | |||
| аммиака и ионов аммония в воде | |||
| Окрашивание при рассмотрении | Аммиак и ионы аммония | ||
| сбоку | сверху | мг азота/л | мг NHJ/л |
| Нет | Нет | 0,04 | 0,05 |
| Нет | Чрезвычайно | 0,08 | 0,1 |
|
| слабо-желто- |
|
|
|
| ватое |
|
|
| Чрезвычайно | Слабо-желто- ватое | 0,2 | 0,3 |
| слабо-желтоватое |
|
| |
|
|
| ||
| Очень слабо-желтоватое | Желтоватое | 0,4 | 0,5 |
|
|
| ||
| Слабо-желтоватое | Светло-желтое | 0,8 | 1,0 |
|
|
| ||
| Желтое | Буровато- | 2,0 | 2,5 |
|
| желтое |
|
|
| Мутноватое, | Бурое, раствор | 4,0 | 5,0 |
| резко-желтое | мутный |
|
|
| Интенсивно- | Бурое, раствор | Более | Более |
| бурое, раствор | мутный | 10,0 | 10,0 |
| мутный |
|
|
|
Определение хлоридов и сульфатов
Концентрация хлоридов в водоемах — источниках водоснабжения допускается до 350 мг/л.
В водах рек северной части России хлоридов содержится обычно немного, не более 10 мг/л, в южных районах — до десятков и сотен мг/л. Много хлоридов попадает в водоемы со сбросами хозяйственно-бытовых и промышленных сточных вод. Этот показатель весьма важен при оценке санитарного состояния водоема.
Качественное определение хлоридов с приближенной количественной оценкой проводят следующим образом. В пробирку отбирают 5 мл исследуемой воды и добавляют 3 капли 10 %-ного раствора нитрата серебра. Приблизительное содержание хлоридов определяют по осадку или помутнению (табл. 5).
Качественное определение хлоридов проводят титрованием пробы анализируемой воды нитратом серебра в присутствии хромата калия как индикатора. Нитрат серебра дает с хлорид-ионами белый осадок, а с хроматом калия — кирпично-красный осадок хромата серебра. Из образовавшихся осад ков меньшей растворимостью обладает хлорид серебра.
| таблица 5 хлоридов | ||
| Осадок или помутнение |
| Концентрация хлоридов, иг/л |
| Опалесценция или слабая муть Сильная муть Образуются хлопья, но осаяедаются не сразу Белый объемистый осадок |
| 1-10 10-50 50-100 Более 100 |
Поэтому лишь после того, как хлорид-ионы будут связаны, начинается образование красного хромата серебра. Появление слабо-оранжевой окраски свидетельствует о конце реакции. Титрование можно проводить в нейтральной или слабощелочной среде. Кислую анализируемую воду нейтрализуют гидрокарбонатом натрия.
В коническую колбу помещают 100 мл воды прибавляют 1 мл 5 %-ного раствора -—хромата калия и титруют 0,05 н. раствором нитрата серебра при постоянном взбалтывании до появления слабо-красного окрашивания.
Содержание хлоридов (X) в мг/л вычисляют _ц0 формуле 1,773 • У-1000
100
где 1,773 — масса хлорид-ионов (мг), эквивалентная 1 мл точно 0,05 н. раствора нитрата серебра; V— объем раствора нитрата серебра, затраченного на титрование, мл.
Качественное определение сульфатов с приближенной количественной оценкой проводят так. В пробирку вносят 10 мл исследуемой воды, 0,5 мл соляной кислоты (1:5) и 2 мл 5 %-ного раствора хлорида бария, перемешивают. По характеру выпавшего осадка определяют ориентировочное содержание сульфатов: при отсутствии мути концентрация сульфат-ионов менее 5 мг/л; при слабой мути, появляющейся не сразу, а через несколько минут, — 5-10 мг/л; при слабой мути, появляющейся сразу после добавления хлорида бария, — 10-100 мг/л; сильная, быстро оседающая муть свидетельствует о достаточно высоком содержании сульфат-ионов (более 100 мг/л).
Определение остаточного хлора в водопроводной воде
Для обеспечения надежности обеззараживания воды необходимо, чтобы после завершения процесса хлорирования в ней содержалось 0,3-0,5 мг/л свободного остаточного хлора.
В коническую колбу вместимостью 500 мл наливают 250 мл водопроводной f воды (перед отбором пробы воды следует пропускать ее из крана длительное время), ; 10 мл буферного раствора с рН 4,6 и 5 мл i 10 %-ного раствора иодида калия. Затем выделившийся иодид тируют раствором тиосульфата натрия до бледно-желтой окраски , приливают 1 мл 1 %-ного раствора крахмала и титруют раствор до исчезновения синей окраски.
Содержание остаточного хлора в воде (X) -вычисляют по формуле
v VrK— 0,177 -1000 , X = -1———(Мг/л),
где 7] — объем 0,005 н. раствора тиосульфата натрия, израсходованного на титрование, мл; К — поправка к концентрации тиосульфата; 0,177 — масса активного хлора, соответствующая 1 мл 0,005 н. раствора тиосульфата натрия, мг; V — объем воды, взятой для анализа, мл.
Приготовление буферного раствора. Для приготовления буферного ацетатного раствора с рН = 4,6 смешивают 102 мл 1 М раствора уксусной кислоты (60 г 100 %-ной кислоты в 1 л воды) и 98 мл 1 М раствора ацетата натрия (136,1 г кристаллической соли в 1 л воды) и доводят объем до 1 л прокипяченной дистиллированной водой.
Качественное обнаружение катионов тяжелых металлов
Обнаружение свинца
В пробирку с пробой воды вносят по 1 мг 50 %-ного раствора уксусной кислоты и перемешивают. Добавляют по 0,5 мл 10 %-ного раствора дихромата калия, при наличии в исследуемой пробе ионов свинца выпадает желтый осадок хромата свинца. Пробирку встряхивают и через 10 мин
прибавляютяют по капле раствора хлорида железа (III) и по капле 0,2 М раствора тиосульфата натрия, перемешивают стеклянной палочкой и сравнивают скорость обесцвечивания обеих проб.
В холостом опыте наблюдается медленное обесцвечивание интенсивно окрашенного в фиолетовый цвет комплексного аниона ; присутствии же ионов меди, играющих роль катализатора, фиолетовый раствор обесцвечивается моментально.
Обнаружение фенолов
Фенол и его производные — сильные яды. Механизм отравления таков: блокируются сульфгидрильные группировки жизненно важных ферментов, а в итоге нарушаются окислительно-восстановительные реакции в клетках организма.
ПДК фенола варьирует от 0,1 мг/л в не-хлорированной воде до 0,001 мг/л в хлорированной. Такая разница неслучайна, так как основной метод обеззараживания воды в нашей стране — хлорирование. При этом фенол, если он присутствует в воде, превращается в пентахлорфенол (в 250 раз более токсичный, чем фенол) и 2,4,6-трихлорфенол (канцероген). Дальнейшее превращение этих веществ ведет к диоксинам. Фенол может образовываться в водоемах при гниении остатков древесины. В воде фенол интенсивно поглощает кислород, возникают заморы, вода становится неприятной на вкус, а рыба, накапливая фенол в тканях, превращается в несъедобную.
Качественное определение фенола проводят следующим образом. В коническую колбу вместимостью 200 мл вносят 100 мл исследуемой воды, затем добавляют раствор хлорной извести или хлорную воду в небольшом объеме. Через 10 мин определяют (сначала на холоде, потом при нагревании), появился ли характерный для хлорфенолов «аптечный» запах.
Приложение 2
Приложение 3
Санитарно-гигиенические исследования воды из водопровода д. Усвятье
| Определяемые показатели | Результаты исследований | Гигиенический норматив | Единицы измерения | |
| 1 | запах | 4 | Балл | |
| 2 | привкус | Не более 2 | Балл | |
| 3 | цветность | 20 (35) | Балл | |
| 4 | мутность | 1,0 | 2,6 | ЕМФ |
| 5 | азот аммонийный | Не более 1,5 | Мг/дм | |
| 6 | нитрит-ион | Не более3,3 | Мг/дм | |
| 7 | нитраты | 30,0 | Не более 45 | Мг/дм |
| 8 | Общая жесткость | 9,0 | 7-10 | Моль/дм |
| 9 | хлориды | Не более 350 | Мг/дм | |
| 10 | железо | 0,4 | Не более 0,3-1 | Мг/дм |
| 11 | фториды | 1,0 | Не более 1,5 | Мг/дм |
| 12 | рН | 7,0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Приложение 4
Санитарно-гигиенические исследования воды
из реки Ужа в районе д. Усвятье
| Определяемые показатели | Результаты исследований | Гигиенический норматив | Единицы измерения | |
| 1 | запах | 2 | 4 | Балл |
| 2 | привкус | — | Не более 2 | Балл |
| 3 | цветность | 20 (35) | Балл | |
| 4 | мутность | 1,0 | 2,6 | ЕМФ |
| 5 | азот аммонийный | 2 | Не более 1,5 | Мг/дм |
| 6 | нитрит-ион | 3,5 | Не более3,3 | Мг/дм |
| 7 | нитраты | 46 | Не более 45 | Мг/дм |
| 8 | Общая жесткость | 4,8 | 7-10 | Моль/дм |
| 9 | хлориды | Не более 350 | Мг/дм | |
| 10 | железо | 0,1 | Не более 0,3-1 | Мг/дм |
| 11 | фториды | 0,3 | Не более 1,5 | Мг/дм |
| 12 | рН | 8,3 |
|
|
