Муниципальное бюджетное образовательное учреждение «Актанышская средняя общеобразовательная школа №1»
Актанышского муниципального района Республики Татарстан
Химия
10 класс
Тема урока: Алканы, получения, свойства и применение
Тип урока: изучение нового материала
Форма урока: урок – путешествие с применением компьютера (с использованием мультимедиа- средств обучения)
Автор: Валиева Эльвира Фанисовна
Тема урока: Алканы, получения, свойства и применение
Урок – путешествие с мультимедийным сопровождением
I. Цели урока.
1. Развивающие цели.
Развивать у школьников логическое мышление, сформировать умение составлять уравнения реакции с участием алканов.
Формировать интеллектуальные умения: умения анализировать свойства алканов, выделять главное, сравнивать, обобщать и систематизировать.
Развивать волю и самостоятельность. Развивать умение владеть собой: уверенность в своих силах, умение преодолевать трудности в учении химии.
2. Образовательные цели.
Обеспечить усвоение учащимися химических свойств и способов получения алканов.
Обобщить и закрепить, систематизировать, ранее полученные знания по видам гибридизации, по номенклатуре органических соединений.
Формировать навыки работы с игровыми элементами, видеофрагментами, иллюстративными материалами.
Формировать культуру здоровья на уроках химии.
Выявить недостаточно освоенные темы и скорректировать учебный процесс и готовить учащихся к ЕГЭ.
3. Воспитательные цели.
Воспитывать культуру речи учащихся.
Воспитать экологическую культуру и мышление у учащихся.
II. Тип урока: изучение нового материала.
III. Вид урока: урок с применением компьютера (с использованием мультимедиа- средств обучения).
IV. Инновационные, информационные технологии обучения, основанные на применении современной передовой техники – компьютеров, интерактивной доски, проектора.
V. Методы урока:
А. Иллюстративно-игровой
Б. Преподавания – сообщающий.
обучения – а/ программированный б/ иллюстративно игровой
2)преподавания – а/ объяснительный б/ стимулирующий 3) учения – а/ репродуктивный б/ частично поисковый
VI. Средства: Компьютер, иллюстративный материал,
игровые элементы, лабораторные опыты и демонстрация на видео.
Х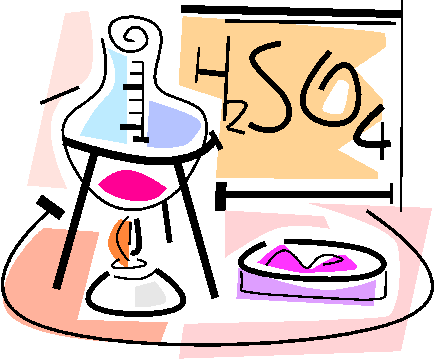 од урока:
од урока:
На экране проектора:
Карта путешествия по стране «Алканы»

Информационная Привал




Разминка Информационная
С
 тарт CnH2n+2
тарт CnH2n+2


 Техника
Техника
 безопасности
безопасности
Финиш Эксперимент
I станция. Разминка. Старт.
1. Устный опрос
1. Бензин, бытовой газ, растворители, пластмассы, красители, спирты, лекарства, духи – все продукты …
2. Болотный газ. Образуется при гниении, при сухой перегонке угля. Является главной составной частью природных газов…
3. Сколько видов органических веществ?
4. из него делают расчески, украшения, бильярдные шары, игрушки, мячи, щетки …
5. Материал для изготовления чемоданов…
6.Многие известные душистые вещества относятся к классу…
7.Всемирно известные духи – французские «Суар де Пари» и «Шанель» изготовлены из каких веществ?
8. Топливо для организма…
9. Это вещество наркотик, не безвреден для человека, парализует нервную, сердечно-сосудистую систему, печень …
10. Кто открыл теорию строения органических соединений?
11. Кто ввел понятие «гибридизация»
12. Что такое изомеры?
2. На экране проектора вопросы и задания
Ученики отвечают. После ответа учеников компьютер сразу дает правильный ответ.
1. Сколько электронов на втором уровне атома углерода.
2. Распределите электроны по орбиталям углерода в возбужденном состоянии.
3. Гибридизация атомных орбиталей.
а) Какие электроны перекрываются?





б) Образование ковалентных связей в молекуле метана (медикация)
в) Образование Г и П связей в молекуле этилена (медикация)
г) Образование Г и П связей в молекуле ацетилена (медикация)
д



 ) Расположение С атомов в пространстве (медикация)
) Расположение С атомов в пространстве (медикация)
4. К какому классу относятся следующие соединения?

 O O
O O
R


 -OH, R-C , R-C , R-O-R, R-CI
-OH, R-C , R-C , R-O-R, R-CI
OH H
5. Общие формулы каких соединений изображены?
CnH2n+2, CnH2n, CnH2n-2,
CnH2n+1COOH, CnH2n+1COH
6.Что такое гомологический ряд? Изображение на экране





 H H H H H H H H H
H H H H H H H H H







 H—C — C—H H—C—C—C—H H—C—C—C—C—H
H—C — C—H H—C—C—C—H H—C—C—C—C—H




H H H H H H H H H
7. Какая формула лишняя ?
C2H6 CH4 C6H16 C16H34 C2H4 C12H24 C4H10
3. Вспомним алгоритм называния веществ ациклического строения.
На экране формула вещества:
H 3C
3C
 CH—CH2—CH3
CH—CH2—CH3
H3C
Медикация с озвучиванием:
1. Выберите самую длинную углеродную цепь
2. Пронумеруйте её с той стороны, к которой ближе радикалы, или старший заместитель, или кратная связь.
( на экране происходит нумерация)
3. Указать в префиксе положения.(номер атома углерода) и назвать радикалы, заместителя, функциональной группы в алфавитном порядке.(на экране 2 – метил -)
4.Назвать основной углеводород (на экране 2-метил- бутан)
5.Если есть двойная связь, то после корня поставить суффикс –ен, для тройной связи -ин, если кратных связей нет – суффикс – ан.
II Информационная станция
1. Физические свойства алканов.
На экране схемы;
Учитель рассказывает: к метану специально добавляют серосодержащие соединения – меркаптаны, для того, чтобы люди могли по запаху определить утечку.
Демонстрация веществ: гексана, парафина
Разветвленные алканы кипят при более низких температурах, чем прямые.
Пишут в тетради: C1 — C4 газы
CH4 — ↑ Tпл = -182,5 °С
C5 – C15 — жидкости
С16 – Сn — твердые
2. Способы получения алканов.
Алканы в больших количествах получают из природного газа и нефти.
Из простых веществ в электрическом разряде:
C+2H2→CH4
Гидролиз карбида алюминия
+3 -4
AI4C3+6HOH → 4AI(OH)3+3CH4↑
Нагревание моногалогеноалканов с металлическим натрием (реакция Вюрца)
C2H5Br+2Na+Br-C2H5 → C2H5 — C2H5 + 2NaBr
Если разные галогеноалканы, то результатом будет смесь трех продуктов: t°
3CH3Br + 3Na + 3Br-C2H5→CH3-CH3 + CH3-CH2-CH3 +C2H5-C2H5
5. Декарбоксилирование. Сплавление ацетата натрия со щелочью. Полученный этим способом алкан будет иметь на один атом углерода меньше. Демонстрация опыта на экранекомпьютера (с озвучиванием)
6. Гидролиз реактива Гриньяра:
7.Алканы симметричного строения могут быть получены в результате электролиза солей карбоновых кислот (реакция Кольба)
III. Станция Привал. (Ученики отдыхают, слушают музыку).
IV. Информационная станция.
3. Химические свойства алканов.
Так как связи в алканах малополярные, то для них характерны радикальные реакции, реакции замещения.
1.Реакции замещения.
а) С галогенами (галогенирование). С хлором на свету, с бромом при нагревании.
В случае избытка хлора хлорирование идет дальше, до полного замещения атомов водорода.
Реакция идет по радикальному механизму.
2.Реакции отщепления
а) Дегидрирование (отщепление водорода)
б) Крегинг алканов:
Крекинг -0 радикальный разрыв связей С-С. Протекает при нагревании и в присутствии катализаторов. При крекинге образуется смесь алканов с меньшим числом С атомов. Механизм свободно радикальный. Этот процесс является важнейшей стадией переработки нефти.
в) при температуре 1500С метан пиролизуется
г) при температуре 1000С:
3 Реакции окисления.
а) В присутствии избытка кислорода происходит полное сгорание алканов до СО2 и Н2О. При сгорании алканов выделяется большое количество теплоты, на этом основано их применение в качестве топлива.
V.Экспериментальная станция
— На экране видеофрагмент с озвучиванием «Горение метана» с озвучиванием:
Низкие алканы горят бесцветным пламенем, а с ростом числа атомов углерода в молекуле пламя алканов становится все более окрашенным и коптящим.
VI. Станция Техника безопасности
а) Газообразные углеводороды с воздухом в определенных соотношениях могут взрываться!
б) В условиях недостатка кислорода происходит неполное сгорание, продуктом является сажа (С) ядовитый газ СО
в) При мягком окислении алканов кислородом воздуха на катализаторах могут быть получены спирты, альдегиды, кислоты с меньшим количеством атомов углерода в молекуле.
4 Реакции изомеризации
Алканы нормального строения при нагревании в присутствии катализатора могут превращаться в алканы с разветвленной цепью.
5. Ароматизация.
Алканы с шестью и более атомами углерода вступают в реакцию дегидрирования с образованием цикла:
Станция Финиш-закрепление
Вопросы по группам.
Домашнее задание:
Упражнение4,6,7,8(писменно),стр.81.
