Сидорина Г.Н.,учитель химии,
Г У. Средняя общеобразовательная школа N 5, г. Актау
Тема урока: «Кальций и его соединения»
(9 класс)
Цель урока:
— дать характеристику кальцию и его соединениям;
— научить учащихся доказывать некоторые свойства кальция и его соединений
при осуществлении химического эксперимента;
— развивать критическое мышление, умение анализировать полученное решение;
коммуникативные способности;
— воспитывать сознательное отношение к учению, научить ценить время урока.
Методы обучения: словесный, наглядный, демонстрационный, практический.
Форма организационно-учебной деятельности: работа в группах(дифференцированная: уровень А(вариант-1), В(вариант-2), С(вариант-3), индивидуальная.
Оборудование: кальций, СаО, Н2О, индикаторы, р- р Са(ОН)2, H2SO4,СО2, пробирки,
интерактивная доска.
Этапы урока
Вводная часть: сообщение темы, постановка целей и задач урока (на интерактивной доске).
Актуализация: проверка домашней работы, интерактивный химический диктант на тему
«Химические свойства металлов».
Основная часть: изучение новой темы.
1.Работа по алгоритму (написано на интерактивной доске):
а) положение металла в ПСХЭ Д.И.Менделеева, строение его атома;
б) физические и химические свойства металла – простого вещества;
в) соединения: оксиды, гидроксиды, соли;
г) применение металла и его соединений;
д) биологическая роль металла.
2.Работа в группах, дифференцированная. Учащиеся получают карточки с заданиями.
Отвечают на вопросы, проводят химический эксперимент ( лабораторные опыты).
В процессе выполнения работы сами комментируют опыты, записывают уравнения
реакций (напоминаем правила техники безопасности).
Опыты.
Отношение кальция к воде (демонстрирует учитель).
Оксид кальция с водой.
Исследование полученных растворов с помощью индикаторов.
Известковая вода + ф/ф.
Известковая вода + углекислый газ до появления осадка и до его исчезновения.
Известковая вода с ф/ф + Н2SO4 → … + …
СаО + НСI → … + …
Варианты заданий
Вариант 1. Задание 1. а) при нагревании в струе водорода кальций соединяется с водородом.
Как называется это соединение? Напишите уравнение реакции.
б) гидрид кальция реагирует с водой, напишите уравнения реакций, укажите, что является
окислителем, восстановителем (обратите внимание на знак зарядов у ионов водорода в гидриде
и воде).
Задание 2. а) приведите уравнения реакций, в которых 1) кальций окисляется; 2) кальций восстанавливается; 3) валентность кальция не меняется.
б) в качестве дефолианта (вещества,способствующего сбрасыванию листьев перед
уборкой хлопчатника), применяется цианамид кальция. Определить формулу этого вещества,
если он содержит Са-50% ; С-15% ; N-35% .
Вариант 2.Задание 1. Сравните химические свойства щелочных металлов со свойствами
кальция. В чем их сходство? Различие? Напишите уравнения реакций для натрия, кальция.
Задание 2. Как осуществить следующий ряд превращений:
а) Са → СаО → Са(ОН)2 → СаСО3 → Са(НСО3)2 ;
б) Са → Са(ОН)2 → СаСО3 → СаО → СаСI2.
Вариант 3. Задание 1. а) зарисуйте схемы строения атомов калия и кальция. Что общего в их строении и в чем различие?
б) какой вывод можно сделать об их химической активности?
Задание 2. а) докажите, что гидроксид кальция – растворимое основание;
б) как осуществить следующий ряд превращений?
Са → Са(ОН)2 → СаСО3 → Са(НСО3)2
↘ СаSО4
Итог урока
Комментарий домашней работы: стр. N0 7, 10,11.
Выставление оценок
Рефлексия Знаю.
Узнал сегодня. Какие трудности были при выполнении работы?
Хочу узнать.
Приложение (интерактивный химический диктант)
Вариант 1
а) Mg + O2 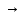 в) Au + O2
в) Au + O2 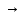 д) Ag + HCI
д) Ag + HCI 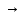
б) Ca + H2SO4 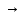 г) Cu + H2O
г) Cu + H2O 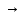 e) Na + H2O
e) Na + H2O 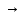
Вариант 2
а) Mg + HCI 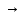 в) Cu + HBr
в) Cu + HBr 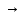 д) Mg + Ca(OH)2
д) Mg + Ca(OH)2 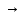
б) Na + I2 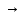 г) Sn + H2O
г) Sn + H2O 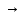 e) Cu + HNO3
e) Cu + HNO3