Урок
Тема: Спирты, строение, номенклатура и изомерия.
Цель:
— познакомить с кислородсодержащими органическими веществами
— дать общую характеристику классу предельных одноатомных спиртов.
Задачи.
Обучающие:
-научить выявлять кислородсодержащие органические вещества по формуле
— научить определять принадлежность вещества к классу предельных одноатомных спиртов
— познакомить с видом химической связи – водородной связью.
Развивающие:
— развитие представлений о генетической связи между классами углеводородов и кислородсодержащими органическими веществами
— развитие умений наблюдать и объяснять физические свойства и химические явления, зависимость свойств веществ от их строения
— развитие интеллектуальных способностей учащихся и их интереса к изучению химии.
Воспитывающие:
— формирование понимания единых принципов организации живой и неживой природы, идеи материального единства веществ природы
— формирование экологического мышления и здорового образа жизни.
ХОД УРОКА
Организационный момент. (1-2 мин)
Цели урока. (1-2)
Мы переходим к изучению нового раздела органической химии «кислородсодержащие органические соединения». К ним относятся жиры, эфиры, карбоновые кислоты и многие другие вещества которые нам предстоит изучить. Простейшим представителем этой группы веществ являются спирты, поэтому они открывают настоящий раздел. На данном уроке нам предстоит познакомиться со строением, изомерией, номенклатурой и классификацией предельных одноатомных спиртов. Научиться составлять их формулы и давать им названия по международной номенклатуре.
III. Активизация знаний учащихся. (5мин)
(беседа)
На предыдущих уроках мы изучали с вами УВ. Из каких элементов состоят данные органические соединения? Чем же отличаются спирты от обычных УВ? Как вы уже поняли, спирты в своем составе содержат кислород и являются производными УВ.
IV. Изучение нового материала. (30-35мин)
Давайте вспомним состав и свойства изученных углеводородов. А теперь проведем небольшой химический диктант. (На столах учащихся карточки с названиями углеводородов. Учитель зачитывает утверждение, учащиеся поднимают соответствующую карточку.
Учитель может выборочно попросить объяснить свой ответ любого учащегося.
1. В названиях имеют суффикс -ан. (Алканы)
2.Для них характерна sp2-гибридизация атомных орбиталей. (Алкены,
диены, арены)
3. В молекулах содержат только сигма – связи. (Алканы, циклоалканы)
4. Имеется одна двойная связь в молекулах. (Алкены)
5. Общая формула этих углеводородов Сп Н2п. (Алкены, циклоалканы)
6.Для них характерны в основном реакции замещения. (Алканы,
циклоалканы)
9.В молекулах обязательно присутствует тройная связь. (Алкины)
10.Для них характерна sp-гибридизация атомных орбиталей. (Алкины)
Затем переходим к изучению нового материала.
Спирты это производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильную группу (-ОН).
1) Гомологический ряд предельных одноатомных спиртов.
Рассмотрим предельные одноатомные спирты. Их общая формула выводится из формулы предельных УВ CnH2n+2, только один атом водорода будет замещен гидроксильной группой –О Н, отсюда общая формула предельных одноатомных спиртов CnH2n+1-ОН. Зная общую формулу предельных одноатомных спиртов можно составить гомологический ряд спиртов.(составление таблицы в тетради и на доске)
Состав спиртов : С,Н,О
Электронная формула: Н Н
. . . . . .
Н : С : С : О :Н
. . . . . .
Н Н
Гидроксильная группа – главная особенность строения спиртов, определяющая их свойства. Кислород гидроксильной группы смещает электронную плотность к себе, связи –О- Н и –С-О – поляризуются.
2) Спирты по-разному классифицируют:
а) В зависимости от валентности спиртовой группировки спирты бывают: первичные – содержат одновалентную спиртовую группировку –СН₂ОН (например, СН₃-СН₂ОН этанол); вторичные – содержат двухвалентную спиртовую группировку =СНОН (например, СН₃-СНОН-СН₃ пропанол-2); третичные – содержат трехвалентную спиртовую группировку =С-ОН (например, 2-метилбутанол-2)
б) По характеру углеводородного радикала спирты бывают: предельные – углеводородный радикал содержит только одинарные связи (например, СН3ОН метанол, С₄Н₉ОН бутанол); непредельные – содержат ненасыщенный углеводородный радикал (например, СН₂=СН-СН₂ОН аллиловый спирт); ароматические – содержат ароматический углеводородный радикал (например, С₆Н₅-СН₂ОН бензиловый спирт).
в) По количеству гидроксильных групп различают спирты: одноатомные – содержат одну ОН-группу (например, СН₃-СН₂₂ОН этанол); двухатомные – содержат две ОН-группы (например, НО-СН₂-СН₂-ОН этиленгликоль или этандиол-1,2); трехатомные – содержат три ОН-группы в молекуле (например, НО-СН₂-СНОН-СН₂-ОН глицерин или пропантриол-1,2,3).
г) По количеству атомов углерода в молекуле спирта: низшие – содержат от 1 до 10атомов углерода в молекуле; высшие – содержат более 11 атомов углерода. (Из представленных ранее формул учащиеся находят спирты формулы спиртов разных классификаций)
–С- О – поляризуются.
3) Изомерия :
Для спиртов характерно несколько видов структурной изомерии:
1.структурная
а) изомерия углеродного скелета,
б) изомерия положения группы –ОН,
2. межклассовая изомерия.
(рассмотреть примеры у доски вещество с формулой С4Н10О)
Пример: СН3-СН2-СН2-СН2-ОН бутанол-1
а) СН3-СН-СН2-ОН 2-метилпропанол-1
|
СН3
б) СН3-СН2-СН-СН3 бутанол-2 С4Н10О
│
ОН ОН
│
СН3-С-СН3 2-метилропанол-2
│
СН3
в) СН3—O— СН2—— СН2— СН3 метилпропиловый эфир
С2Н5—O— С2Н5 диэтиловый эфир (названия веществам дать после рассмотрения номенклатуры, определить, где первичные, и вторичные, третичные спирты)
(показать на примере шаростержневых моделей
4) Номенклатура :
Тривиальная номенклатура – названия спиртов происходят от названий радикалов: СН₃ОН – метиловый спирт.(С₂Н₅ОН,С₃Н₇ОН – называют самостоятельно.) Систематическая номенклатура – названия спиртов образуются из названий предельных углеводородов добавлением суффикса –ол: СН₃ОН – метанол. Основные принципы номенклатуры спиртов: Выбирают самую длинную углеродную цепь и нумеруют с того конца цепи, к которому ближе находится гидроксо-группа. Называют заместители в основной углеродной цепи и цифрами указывают их положения. Называют основную цепь как алкан и добавляют суффикс –ол. Цифрой указывают положение ОН-группы.
5) Физические свойства спиртов:
Агрегатное состояние:
С1-С11— жидкости
С12-С…- твердые вещества.
Растворимость в воде: высокая
Растворимость спиртов в воде обусловлена образованием водородной связи между атомами водорода одной молекулы и атомами сильно электроотрицательных элементов (кислорода, фтора) другой молекулы. Вы знаете, что водородная связь обозначается тремя точками.
. . . О — Н … О — Н … О- Н …



R R R
В образовании водородной связи принимает участие атом водорода гидроксильной группы молекулы спирта, поэтому с увеличением УВ радикала растворимость спиртов уменьшается.
V. Закрепление материала проводим в виде теста.
Тест.
1. Общая формула гомологического ряда предельных одноатомных спиртов: Начало формы
1)CnH2n – 1ОН; Прочитайте параграфы § 4.1. Спирты, § 1.1. Классификация органических соединений.2)CnH2n + 1ОН; Прочитайте параграфы § 4.1. Спирты, § 1.1. Классификация органических соединений.3)CnH2n – 3ОН; Прочитайте параграфы § 4.1. Спирты, § 1.1. Классификация органических соединений. 4)CnH2nОН.
2. Предельным одноатомным спиртом не является:
1) метанол
2) 3-этилпентанол-1
3)2-фенилбутанол-1
4) этанол
3. Число изомерных спиртов состава С4Н10О (без оптических изомеров) равно: Начало формы
1)двум; Вы не учли изомерию углеводородного скелета.
Прочитайте параграфы § 4.1. Спирты, § 1.3. Изомерия и ее виды. 2)трем; Прочитайте параграфы § 4.1. Спирты, § 1.3. Изомерия и ее виды. 3)четырем; Прочитайте параграфы § 4.1. Спирты, § 1.3. Изомерия и ее виды. 4)пяти. Прочитайте параграфы § 4.1. Спирты, § 1.3. Изомерия и ее виды.Начало формы
4. Изомером положения функциональной группы для пентанола-2 является:
1) пентанол-1
2) 2-метилбутанол-2
3) бутанол-2
4) 3-метилпентанол-1
5.Тривиальное название метанола: Начало формы
1)винный спирт; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений. 2)древесный спирт; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений. 3)муравьиный спирт;Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений. 4)медицинский спирт.
6. Какой вид химической связи определяет отсутствие среди гидроксисоединений газообразных веществ (при обычных условиях)?
1) ионная
2) ковалентная
3) донорно-акцепторная
4) водородная
7. Температуры кипения спиртов по сравнению с температурами кипения соответствующих углеводородов:
1) примерно сопоставимы;
2) ниже;
3) выше;
4) не имеют четкой взаимозависимости.
8. Тривиальное название этанола: Начало формы
1)алкоголь; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений. 2)питьевой спирт; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений. 3)винный спирт; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений. 4)самогон. Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
9. Выберите верное утверждение:
1) спирты – сильные электролиты;
2) спирты хорошо проводят электрический ток;
3) спирты – неэлектролиты;
4) спирты – очень слабые электролиты.
10. Молекулы спиртов ассоциированы из-за:
1) образования внутримолекулярных связей;
2) образования кислородных связей;
3) образования водородных связей;
4) молекулы спиртов не ассоциированы.
11. При окислении метанола образуется:
1) метан 2) уксусная кислота 3) метаналь 4) хлорметан
12. Какое вещество образуется при нагревании этилового спирта до 140оС в присутствии концентрированной серной кислоты?
1) уксусный альдегид 2) диметиловый эфир 3) диэтиловый эфир 4) этилен
13. Кислотные свойства этанола проявляются в реакции с
1) натрием 2) оксидом меди (II)
3) хлороводородом 4) подкисленным раствором перманганата калия
14. Укажите формулу 3-метилпентанола-2:
Начало формы
![]() Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
![]() Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
![]() Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
![]()
15. Укажите формулу 2,3-диметилпентанола-1:
Начало формы
![]() Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений. ![]()
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
![]() Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
![]()
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
16. Название вещества с формулой 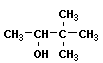 :
:
Начало формы
1)3,3-диметилбутанол-2; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
2)2,2-диметилбутанол-3; Нумерация выбирается так, чтобы номер ОН-группы был минимальным.
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
3)2,2-диметилбутанол-1; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
4)3,3-диметилбутанол-1. Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
17. Название вещества с формулой ![]() :
:
Начало формы
1)2-метилбутанол-4; Нумерация выбирается так, чтобы номер ОН-группы был минимальным
Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
2)3-метилбутанол-1; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
3)3-метилпентанол-1; Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
4)2-метилбутанол-1. Прочитайте параграфы § 4.1. Спирты, § 1.2. Основы номенклатуры органических соединений.
VI. Задание на дом: § 15 упр 1-3. Новошинский И.И., Новошинская Н.С. Органическая химия 10(11) класс. Базовый уровень для общеобразовательных учреждений.
Список используемой литературы.
Программа курса, тематическое и поурочное планирование к учебнику. И.И.Новошинский, Н.С.Новошинская «Химия» для 11 класса общеобразовательных учреждений.-М.: ООО «ТИД «Русское слово-РС»,2008.
Текущий и итоговый контроль по курсу «Химия» 10(11) класс. Базовый уровень /И.И.Новошинский, Н.С.Новошинская «Химия» М.: ООО «ТИД «Русское слово-учебник»,2008.
Органическая химия: пособие для старшеклассников, упражнения, задачи, тесты/ И.И.Новошинский, Н.С.Новошинская «Химия» М.: ООО «ТИД «Русское слово-РС»,2011. ( Готовимся к ЕГЭ)
Переходные элементы и их соединения; теория, упражнения, тесты, задачи, решения: пособие для старшеклассников и абитуриентов/ И.И.Новошинский, Н.С.Новошинская.-Краснодар:Совет.Кубань,2006.
ЕГЭ 2010-2012,:сборники экзаменационных заданий/ Авт.-сост.: А.А.Каверина, Ю.Н.Медведев, Д.Ю.Добротин.-Мю:Эксмо,2010-2012(ЕГЭ. Федеральный банк экзаменационных материалов).
Химия 11 класс Тематические тесты для подготовки к государственной итоговой аттестации-2010:учебно-методическое пособие/Под ред. В.Н.Доронькина. -Ростов н/Д:Легион,2009-( государственная итоговая аттестация)
Сборник самостоятельных работ по химии 11 класс/И.И.Новошинский, Н.С.Новошинская -2-е изд .«Химия» М.: ООО «ТИД «Русское слово-учебник»,2010.
Химия. 11 класс. 52 диагностических варианта/Е.В. Савинкина.- М.Издательство «Национальное образование»,2012.-(ГИА. Э кспресс — диагностика).
Типы химических задач и способы их решения: 8-11 классы И.И.Новошинский, Н.С.Новошинская «Химия» М.: ООО «ТИД «Русское слово-РС»2010-2012. ( Подготовка к ЕГЭ)
