Периодическая таблица химических элементов. Строение атома
1 вариант
Атом – сложная:
Положительно заряженная частица
Электронейтральная частица
Отрицательно заряженная частица
Античастица
Порядковый номер химического элемента показывает на:
Массу атома
Число частиц в ядре
Количество энергетических уровней
Величину заряда ядра
Химический элемент – это вид атомов с одинаковым:
Количеством нейтронов
Зарядом ядра
Массой
Количеством электронов
Число электронов в атоме фтора равно:
9
19
10
28
Номер периода показывает:
Массу атома
Число электронов на внешнем энергетическом уровне
Количество энергетических уровней
Величину заряда ядра
Протон – частица, которая:
Несет положительный заряд
Несет отрицательный заряд
Электронейтральна
Может иметь как положительный, так и отрицательный заряд
Номер группы показывает:
Общее количество электронов
Число энергетических уровней
Количество электронов на внешнем энергетическом уровне
Число протонов
Масса атома сосредоточена в:
Электронах
Протонах
Нейтронах
Ядре
Количество частиц в атоме CI (изотоп  ):
):
P+ ― 17 n0 – 35 ē – 17
P+ ― 35 n0 – 17 ē – 17
P+ ― 17 n0 – 18 ē – 17
P+ ― 18 n0 – 17 ē – 35
В группе элементов: Na, Mg, AI, Si металлические свойства более выражены у:
Mg
AI
Na
Si
2 вариант
Химический элемент – это вид атомов с одинаковым:
Количеством нейтронов
Количеством электронов
Зарядом ядра
Массой
Атом – сложная:
Электронейтральная частица
Отрицательно заряженная частица
Античастица
Положительно заряженная частица
Порядковый номер химического элемента показывает на:
Массу атома
Число частиц в ядре
Величину заряда ядра
Количество энергетических уровней
Масса атома сосредоточена в:
Электронах
Ядре
Нейтронах
Протонах
Число электронов в атоме натрия равно:
23
33
12
11
Номер группы показывает:
Количество электронов на внешнем энергетическом уровне
Общее количество электронов
Число энергетических уровней
Число протонов
Номер периода показывает:
Массу атома
Количество энергетических уровней
Число электронов на внешнем энергетическом уровне
Величину заряда ядра
Количество частиц в атоме O (изотоп 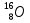 ):
):
P+ ― 8 n0 – 8 ē – 16
P+ ―16 n0 – 8 ē – 8
P+ ―16 n0 – 8 ē – 8
P+ ― 8 n0 – 8 ē – 8
В группе элементов: K, Ca, Fe, Br металлические свойства более выражены у:
Br
Ca
K
Fe
Электрон – частица, которая:
Несет положительный заряд
Несет отрицательный заряд
Электронейтральна
Может иметь как положительный, так и отрицательный заряд
